
科目: 来源: 题型:
在100℃时,将0.40mol的二氧化氮气体充入2L抽空的密闭容器中,发生反应:
2NO2![]() N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目: 来源: 题型:
A、T、X、Y、z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:
| 元素 | 结构或性质信息 |
| T | 基态原子的L层上s电子数等于p电子数 |
| X | 基态原子最外层未成对电子数在该元素所在周期中最多 |
| Y | 基态原子的第一电离能在该元素所在周期中最小 |
| Z | 单质常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
请根据信息回答有关问题(答题时如需表示具体元素,请用相应的元素符号):
(1)T、X、Z三种元素的电负性由大到小的顺序是 。
(2)写出与x单质分子互为等电子体的物质的化学式 、 。
(分子、离子各一种)
(3)元素Q的原子序数是Y与Z的原子序数之和。
①元素Q与元素T、x能形成平面型的[Q(TX)4]2-离子。TX-中T原子采用的轨道杂化方式是 。
②Q单质的晶胞如图所示,Q单质中Q原子的配位数为 。
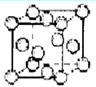
![]()
查看答案和解析>>
科目: 来源: 题型:
在容积为2.0 L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题:

(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为____。
(2)根据右图写出该反应的化学方程式_______,该反应的平衡常数表达式为K=__________。
(3)第5分钟时,升高温度,A、B、D的物质的量变化如右图,则该反应是_____(填“放热”或“吸热”)反应,反应的平衡常数____(填“增大”、“减小”或“不变”。下同),B的反应速率______。若在第7分钟时增加D的物质的量,A的物质的量变化正确的是_____(用图中a~c的编号回答)
(4)某同学在学习了“化学反应速率和化学平衡”专题后,发表如下观点,你认为错误的是___。
a.化学反应速率理论是研究怎样在一定时间内快出产品
b.化学反应速率理论是研究怎样提高原料转化率
c.化学平衡理论是研究怎样使用有限原料多出产品
d.正确利用化学反应速率和化学平衡理论都可以提高化工生产的综合效益
查看答案和解析>>
科目: 来源: 题型:
下列物质之间的相互转化不符合![]() (“→”表示一步反应的是)
(“→”表示一步反应的是)
| 甲 | 乙 | 丙 | |
| A | Si | SiO2 | H2SiO3 |
| B | CH3CH2OH | CH3CH2Br | CH2==CH2 |
| C | AlCl3 | NaAlO2 | Al(OH)3 |
| D | HClO | Cl2 | HCl |
查看答案和解析>>
科目: 来源: 题型:
现有A、B、C、D、E、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构。已知:
①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:
 G P Q M+P ;
G P Q M+P ;
④E和D是同主族元素,二者能形成微粒的个数比为1:2和1:3的化合物T和K;
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y。
请回答下列问题:
(1)B元素的名称是 ▲ ;(2)E元素的原子结构示意图是 ▲ 。
(3)请将C的元素符号填在如图所示的元素周期表的适当位置上。
|