
科目: 来源: 题型:
元素性质呈现周期性变化的根本原因是 ( )
A.元素的相对原子质量递增,量变引起质变
B.元素的原子半径呈周期性变化
C.元素原子的核外电子排布呈周期性变化
D.元素的化合价呈周期性变化
查看答案和解析>>
科目: 来源: 题型:
下列变化,是通过取代反应来实现的是
A.CH3CH2OH →CH3CHO B.CH2=CH2 → CH3-CH2Br
C.苯→硝基苯 D.CH3COOH → CH3COOC2H5
查看答案和解析>>
科目: 来源: 题型:
下列是由A→D的反应路线图

(1)写出反应①的化学方程式 。
(2)三步反应中属于取代反应的有 (填反应序号)。
(3)D有多种同分异构体,其中含有 基团的同分异构体有 (不含D)。
基团的同分异构体有 (不含D)。
a.5种 b.6种 c.7种 d.8种
查看答案和解析>>
科目: 来源: 题型:
聚碳酸酯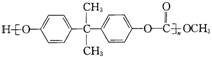 透光率好,可制作车、船、飞机的挡风玻璃。它是由碳酸二甲酯 CH3O-CO-OCH3 与下列那种物质缩聚而成的?
透光率好,可制作车、船、飞机的挡风玻璃。它是由碳酸二甲酯 CH3O-CO-OCH3 与下列那种物质缩聚而成的?
A.二卤化物 B.二酚类 C.二醛类 D.二烯类
查看答案和解析>>
科目: 来源: 题型:
德国克莱斯公司成功研制了利用甲醇车载制氢氧燃料电池工艺,其原理如右图所示,请观察此图回答:

(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H= + 49.0 kJ·mol-1
②2CH3OH(g)+O2(g)=2CO2(g)+4H2(g);△H=-385.8kJ·mol-1
下列说法正确的是
A.反应①中反应物的总能量高于生成物的总能量
B.反应①中拆开CH3OH(g)和H2O(g)中的化学键所需能量大于形成CO2(g)和3H2(g) 中的化学键所释放的能量
C.CH3OH蒸气的燃烧热为大于192.9 kJ·mol-1
D.根据②推知反应:2CH3OH(l)+ O2(g)=2CO2(g)+4H2(g)的△H>-385.8kJ·mol-1
(2)最近科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为可再生燃料甲醇。若有2.2kg CO2与足量H2恰好完全反应,生成气态的水和甲醇,可放出2473.5 kJ的热量,试写出合成塔中发生反应的热化学方程式 。
(3)可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如右图。甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O。b处通入的物质是 ,负极反应为: 。

查看答案和解析>>
科目: 来源: 题型:
如下图所示,三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1)中红棕色变深,(3)中红棕色变浅,下列叙述正确的是

A.2NO2![]() N2O4 是放热反应 B.NH4Cl溶于水时放出热量
N2O4 是放热反应 B.NH4Cl溶于水时放出热量
C.烧瓶(1)中平衡混合气的相对分子质量增大 D.烧瓶(3)中气体的压强增大
查看答案和解析>>
科目: 来源: 题型:
l8图中电极a、b分别为Ag电极和Pt电傲,电极c、d都是石墨电极。通电一段时间后,在c、d两极共收集到336mi。(标准状况)气体,其体积比为l:2。回答:

(1)直流电源中,M为 极。
(2)b电极上的电极反应方程式 ,c电极上的电极反应方程式 。
(3)通电一段时间,AgNO3溶液的pH(填”增大”、”减小”或”不变”。) 。
(4)若通电一段时间后H2SO4溶液的质撮分数由5.00%变为5.02%,则原5.00%,的H2SO4溶液为 g。(保留三位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com