
科目: 来源: 题型:
氯化铁溶液与氢氧化铁胶体具有的共同性质是
A.分散质颗粒直径都在l~100nm之间 B.能透过半透膜
C.加入浓氢氧化钠溶液都产生红褐色沉淀 D.颜色都呈红褐色
查看答案和解析>>
科目: 来源: 题型:
强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O(l)△H
=-57.3KJ·mol-1。分别向1L 0.5mol·L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是()
A.△H1>△H2>△H3 B.△H1<△H2<△H3
C.△H1>△H2=△H3 D.△H1=△H2<△H3
查看答案和解析>>
科目: 来源: 题型:
如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).
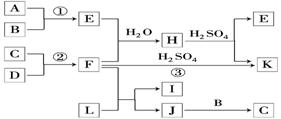
已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式_______________________________________________.
(2)C的结构式__________________________;H的化学式____________________.
(3)L的溶液与化合物E反应的离子方程式:____________________________.
(4)化合物J的化学式____________________.
查看答案和解析>>
科目: 来源: 题型:
钠是一种很活泼的金属,在工业上常用电解熔融NaCl的方法制得,其另一产物氯气的用途也十分广泛,工业上制取漂白粉就是其用途之一。
(1)请写出工业上用电解方法制取钠的化学方程式 。
(2)工业上制取漂白粉的化学反应方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,漂白粉的主要成分是 。
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质。
①提出合理假设。
假设1:该漂白粉未变质,只含 ;
假设2:该漂白粉全部变质,只含 ;
假设3:该漂白粉部分变质, 。
② 设计实验方案,进行实验。请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水。(提示:不必检验Ca2+和Cl-,表格可以不填满。)
| 实验步骤 | 预期现象和结论 | |
| ① | 取少量上述漂白粉于试管中,
|
|
| ② | ||
| ③ | ||
查看答案和解析>>
科目: 来源: 题型:
下列实验过程中,始终无明显现象的是 ( )
A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中
C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba(NO3)2溶液中
查看答案和解析>>
科目: 来源: 题型:
由金红石(TiO2)制取单质Ti,涉及的步骤为:![]()
已知:①C(s)+O2(g)====CO2(g) ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g) ====2CO2(g) ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g) ====TiCl4(s)+O2(g) ΔH=+141 kJ·mol-1
则(1)TiO2(s)+2Cl2(g)+2C(s) ====TiCl4(s)+2CO(g)的ΔH=____________________。
(2)碳在氧气中不完全燃烧生成CO的热化学方程式为_______________________________。
查看答案和解析>>
科目: 来源: 题型:
制造太阳能电池需要高纯度的硅,工业上制高纯硅常用以下反应实现( )
|