
科目: 来源: 题型:阅读理解
阅读下面两条科普信息,回答有关问题:
一个体重50kg的健康人身体中含铁2g,这2g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收:
在新生代的海水里有一种铁细菌,它们提取海水中的亚铁离子,利用酶为催化剂把它转变成它们的皮鞘(可以用Fe2O3来表示其中的铁),后来便沉积下来形成铁矿:该反应的另一种反应物是CO2,反应后CO2转变成有机物(用甲醛CH2O表示)。
(1)这两则科普信息分别介绍了人体内和海水中的亚铁离子与铁离子(或者铁的高价化合物)相互转化的事实、方法和途径。这说明维生素C具有 性,铁离子具有 性,第二则则信息中CO2是 剂。
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
__Fe(NO3)3 +__ NaOH+ __Cl2 → __Na2FeO4+ __NaNO3 + __NaCl + __H2O
①配平上述反应,并分析 元素被氧化,当生成3mol还原产物时,转移电子的总数为 ;
②铁酸钠除了能消毒外,还可以用于净水,原因是 。
查看答案和解析>>
科目: 来源: 题型:
Cu2O是一种半导体材料,基于绿色化学理念设计的制取.Cu2O的电解池示意图如下,点解总反应:2Cu+H2O==Cu2O+H2O![]() 。下列说法正确的是
。下列说法正确的是
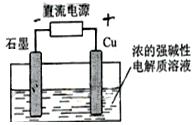
A.石墨电极上产生氢气
B.铜电极发生还原反应
C.铜电极接直流电源的负极
D.当有0.1mol电子转移时,有0.1molCu2O生成。ww.ks5.u.co
查看答案和解析>>
科目: 来源: 题型:
某混合物粉末可能含有Al、Fe、FeO、Al2O3,某研究小组在实验室积极探究其组成。
(1)研究小组首先排除了含有单质Al的可能性,加入的试剂是_______(填序号)
A.硫酸 B.盐酸 C.氨水 D.氢氧化钠溶液
证明不含单质铝的现象是 。
(2) 该混合物的组成基本确定为Fe、FeO、Al2O3。请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3mol/LNaOH、3mol/L盐酸、3% H2O2、3mol/LCuSO4、蒸馏水。
根据你设计的实验方案,在答题卡上按下表的格式写出空白部分的实验操作、预期现象和结论。
| 实验操作 | 预期现象和结论 |
| 步骤1:取少量粉末于烧杯中,加入足量3mol/LNaOH溶液,充分搅拌,过滤,洗涤。 | 粉末减少,说明粉末可能含有Al2O3 |
| 步骤2:取少量步骤1的滤液于试管中,逐滴滴加3mol/L盐酸至过量。 | _____________________________, 说明粉末中含有Al2O3。 |
| 步骤3:将步骤1的滤渣转移到烧杯B中,加入足量3mol/L CuSO4,充分搅拌,过滤,洗涤。 | 有红色固体生成,说明粉末中含有____。 |
| 步骤4:
|
|
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A. 烯烃和烷烃都能发生加聚反应
B.蛋白质水解的最终产物中一定含有肽键
C.乙烯和甲苯都能使酸性高锰酸钾溶液褪色
D.光导纤维、棉花、油脂、树脂都是由高分子化合物组成的物质
查看答案和解析>>
科目: 来源: 题型:
下列表述Ⅰ和Ⅱ都正确,且存在因果关系的是
| 表述Ⅰ(因) | 表述Ⅱ(果) | |
| A | Si和Ge同主族且位于金属和非金属交界线两侧 | Si为非金属元素,其单质是半导体;Ge为金属元素,其单质是导体 |
| B | “硅胶”是硅酸钠的冻状凝胶经脱水后得到的,多孔、吸附水分能力强 | 硅胶常用作实验室和袋装食品、瓶装药品等的干燥剂 |
| C | 打磨过的铝箔在空气中其表面会很快生成Al2O3薄膜,而且Al2O3的熔点高于Al | 打磨过的铝箔在空气中燃烧会失去光泽但熔化的铝并不滴落 |
| D | Fe2O3难溶于水 | Fe(OH)3不能通过化合反应直接制得 |
查看答案和解析>>
科目: 来源: 题型:
下列涉及有机物的说法正确的是:
A.乙烯、氯乙烯、苯乙烯都是不饱和烃,均可用于合成有机高分子材料
B.丙烷是一种清洁燃料,可用作燃料电池的燃料
C.苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴
D.淀粉和纤维素水解产物都是葡萄糖,因此二者互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
把NO2气体装入带活塞的圆筒中慢慢压缩,下列叙述正确的是( )
A.体积减半,压强为原来二倍
B.体积减半,压强增大,但小于原来的2倍
C.体积减半,N2O4的百分含量增大1倍
D.体积减半,则NO2浓度减小
查看答案和解析>>
科目: 来源: 题型:
下列各组物质混合后,不能生成NaOH的是
A.Na和H2O B.Ca(OH)2溶液和NaCl溶液
C.Na2O2和H2O D.Ca(OH)2溶液和Na2CO3溶液
查看答案和解析>>
科目: 来源: 题型:
如下图所示,若电解5min时铜电极质量增加2.16g,试回答:
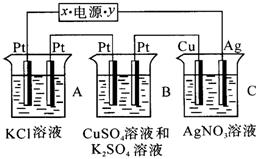
(1)电源电极x名称为 。
(2)pH变化:B ,C 。(填“增大”“减小”或“不变”)
(3)通电5min时,B中共收集到224mL气体(标况),溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为 (设电解前后溶液体积无变化)。
(4)若A中KCl溶液的体积也是200mL,电解后,溶液的pH是________(设电解前后溶液体积无变化)。
查看答案和解析>>
科目: 来源: 题型:
甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料。已知
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △Ha = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H b =-566.0 kJ·mol-1
(1)试写出CH3OH(1)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式:
(2)甲醇作为燃料,它的优点是燃烧时排放的污染物少,从而不仅能缓解能源紧张和温室效应的问题,还能改善大气质量。试利用(1)中的热化学方程式计算,完全燃烧20g甲醇,生成二氧化碳和水蒸汽时,放出的热量为 kJ ,生成的CO2气体标准状况下体积是 L
(3)科研人员新近开发出一种由甲醇和氧气以强碱做电解质溶液的新型手机电池,可使手机连续使用一个月才充一次电,据此回答下列问题:
甲醇在 极反应;电极反应式为 。
(4)利用电池可实现电能向化学能转化。某同学设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)
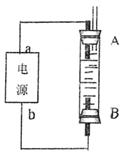
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H+ + 2e-→H2↑
若将所得Fe(OH)2沉淀暴露在空气中,其颜色变化是 ,反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com