
科目: 来源: 题型:
燃烧物质的量相等的某有机物和乙醇,实验测得:
①乙醇燃烧生成的CO2的量是该有机物燃烧生成的CO2的量的2/3;
②该有机物燃烧生成水的量是乙醇燃烧生成水的量的2/3;
③二者消耗相同状态下氧气的体积相同,
通过分析判断该有机物是
A.C4H9OH B.CH2=CHCOOH C.CH2=CHCHO D.CH3CH2COOH
查看答案和解析>>
科目: 来源: 题型:
已知A、E、I、L是常见的非金属单质,其中A为淡黄色固体;Z是常见的金属单质,B的相对分子质量比A大32,C的相对分子质量比B大16,Y是一种常见的液体,J是磁性氧化铁, D、H、K均是重要的化工产品;X分子的球棍模型如图所示,组成X的两种元素的相对原子质量相差18。下列框图中部分反应条件已略去。

试回答下列问题:
(1)下列有关X的说法正确的是 .
A.该物质的分子式为S4N4
B.该物质的分子中既有极性键又有非极性键
C.该物质具有很高的熔、沸点
D.该物质与化合物S2N2互为同素异形体
(2)E的电子式为 ,D的分子式 ,在反应①、②、③、④、⑤、⑥中属于非氧化还原反应的是 。(填序号)
(3)写出反应②的化学方程式: 。
(4)J与过量H的稀溶液反应的离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
在11.2g铁和铜的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成21.4g沉淀,则下列表示X组成的选项中合理的是
A.0.3mol NO2 B.0.3mol NO;0.1mol NO2
C.0.3mol NO2;0.1mol NO D.0.6mol NO
查看答案和解析>>
科目: 来源: 题型:
已知pH为4-5的条件下,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(n)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,过程如下图:
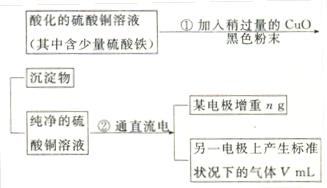
回答下列问题:
(1)加入CuO的作用是 。
(2)步骤②中所用的部分仪器如图所示,则A、B分别连直流电源的 和 极(填“正”或“负”)。
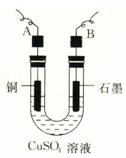
(3)电解开始后,在U形管中可以观察到的现象有: 。A极发生的电极反应式为 。
B极发生的电极反应式为_____________________________________。
(4)下列实验操作中必要的是 (填写字母)。
(A)称量电解前的电极的质量;(B)电解后,电极在烘干称量前,必须用蒸馏水冲洗;(C)刮下电解后电极上析出的铜,并清洗,称量;(D)电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行;(E)在有空气存在的情况下,烘干电极必须用低温烘干的方法。
(5)铜的相对原子质量为 (用带有n、V的式子表示)。
查看答案和解析>>
科目: 来源: 题型:
(8分,每空2分)下图是某药物中间体的结构示意图:


试回答下列问题:
(1)考察上面的结构式与立体模型,通过对比指出结构式中的“Et”表示 (写名称);该药物中间体分子的化学式为 。
(2)你根据结构示意图,推测该化合物所能发生的反应 。
(3)决定有机分子结构问题的最强有力手段是核磁共振氢谱(NMR)。有机化合物分子中有几种化学环境不同的氢原子,在NMR中就有几个不同的吸收峰,吸收峰的面积与H原子数目成正比。现有一种芳香族化合物与该药物中间体互为同分异构体,其模拟的核磁共振氢谱图如上图所示,试写出该化合物的结构简式: 。
查看答案和解析>>
科目: 来源: 题型:
[化学—物质结构与性质]铜是过渡元素。化合物中,铜常呈现+1价或+2价。
(1)右图为某铜矿晶体结构单元,该铜矿的化学式为________。
(2)已知,铜的第一电离能为746kJ·mol-1,第二电离能为
1958kJ·mol-1。请结合核外电子排布相关知识解释,铜第二电离能远
远大于第一电离能的原因![]()
答:____________________________________。
(3)对于CuX(X为卤素)而言,铜与X形成的化学键极性越强,对应的CuX的溶解度越大。据此可知,CuCl的溶解度比CuI的溶解度__________(填“更大”或“更小”)。
(4)CO、NH3都能提供孤电子对与Cu+形成配合物。Cu+与NH3形成的配合物可表示为[Cu(NH3) n]+。该配合物中,Cu+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子对。
①[Cu(NH3)n]+中n =______________________。
②[Cu(NH3) n]+中Cu+与n个氮原子构成的空间结构呈___________型。
③[Cu(NH3) n]+溶液可用于吸收合成氨原料气中的CO,加热吸收CO后的溶液又将放出CO。加热分解放出CO的过程中,必须克服微粒间的哪类作用力?答:______________。
查看答案和解析>>
科目: 来源: 题型:
对于常温下pH为4的醋酸溶液,下列叙述正确的是
A.该溶液的c(H+)为1×10-4 mol·L-1
B.该溶液lmL稀释至100mL后,pH等于6
C.向该溶液中加入等体积、pH为10的氢氧化钠溶液恰好完全中和
D.该溶液中醋酸电离出的c(H+)与水电离出的c(H+)的比值为106
查看答案和解析>>
科目: 来源: 题型:
用石墨电极在一定温度下电解K2SO4饱和溶液m g。当阴极产生a mol气体时,从溶液中析出n g无水晶体。则剩余溶液的溶质质量分数是 ( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
家用液化气中的主要成分之一是丁烷(C4H10)。已知1mol液态水汽化时需要吸收44 KJ热量。(相对原子质量:H—1 C—12 )
(1)当58 Kg丁烷完全燃烧生成CO2和液态水时,放出的热量是3×106 KJ,则丁烷燃烧的热化学反应方程式是 ;
(2)1mol丁烷完全燃烧产生水蒸气时放出的热量为多少KJ?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com