
科目: 来源: 题型:
常温下,向一定浓度的醋酸溶液中逐滴加入氢氧化钠溶液直至过量,在此操作过程中,有关溶液中离子浓度变化的大小关系不正确的是 ( )
A.当pH=7时,c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
B.当pH>7时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.当恰好完全中和时,c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.反应全程都有关系:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
查看答案和解析>>
科目: 来源: 题型:
在一体积固定的密闭容器中进行下列反应:2SO2+O2![]() 2SO3(g),当反应达到平衡时SO2、O2、SO3的浓度分别为0.2 mol·L-1,0.1 mol·L-1,0.2 mol·L-1,则反应起始时的部分物质的数据不可能是
2SO3(g),当反应达到平衡时SO2、O2、SO3的浓度分别为0.2 mol·L-1,0.1 mol·L-1,0.2 mol·L-1,则反应起始时的部分物质的数据不可能是
A.SO2为0.4 mol·L-1,O2为0.2 mol·L-1 B.SO2为0.25 mol·L-1
C.SO2,SO3均为0.15 mol·L-1 D.SO3为0.4 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
如图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略。将该装置放置在有光亮的地方,让混和气体缓慢地反应一段时间。

(1)经过几个小时的反应后,U型管左端产生的现象是: _______、_______、______右端的玻璃管中水柱变化是 。
A.升高 B.降低 C.不变 D.无法确定
(2)试解释U型管右端的玻璃管中水柱变化的原因 。
(3)在反应生成物中:常用作有机溶剂的是_______,常用作灭火剂的是__ ,
______分子只有一种结构的事实能有效证明CH4是 结构而非平面正方形结构。
(4)假设甲烷与氯气充分反应,且只产生一种有机物,请写出化学方程式 。
(5)写出符合下列条件的甲烷的一种同系物的结构简式
A.氢原子数为十八 B.一氯取代物只有一种结构
查看答案和解析>>
科目: 来源: 题型:
下述做法能改善空气质量的是( )
A.以煤等燃料作为主要生活燃料
B.利用太阳能、风能和氢能等能源替代化石能源
C.鼓励私人购买和使用汽车代替公交车
D.限制使用电动车
查看答案和解析>>
科目: 来源: 题型:
25℃时,下列溶液中微粒的物质的量浓度关系正确的是

A.![]() 的
的![]() 与
与![]() 混合溶液中:
混合溶液中:![]()
B.0.1![]() 的KHA溶液,其PH=10 c(K+)﹥c(OH-)﹥c(HA-)
的KHA溶液,其PH=10 c(K+)﹥c(OH-)﹥c(HA-)
C.20mL 0.1![]() 醋酸钠溶液与10mL 0.1
醋酸钠溶液与10mL 0.1![]() 盐酸混合后的溶液中:
盐酸混合后的溶液中:
![]()
D.在25mL 0.1 ![]()
![]() 溶液中逐滴加入0.2
溶液中逐滴加入0.2![]()
![]() 溶液,溶液pH变化如右图所示,在A、B间任一点,溶液中一定都存在下列关系:
溶液,溶液pH变化如右图所示,在A、B间任一点,溶液中一定都存在下列关系:
![]()
查看答案和解析>>
科目: 来源: 题型:
某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积变化的曲线如图所示。据图判断正确的是 ( )

A.Ⅱ为盐酸稀释时pH变化曲线
B.a点KW的数值比c点KW的数值大
C.b点溶液的导电性比c点溶液的导电性强
D.b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
科目: 来源: 题型:
[选修一物质结构与性质]
有X、Y、Z、Q、M 、E、N、G前四周期且原子序数递增的八种元素,其中X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素基态原子核外有两个电子层,最外层有3个未成对电子,Q的基态原子核外成对电子数是成单电子数的3倍,E原子得到一个电子后3p轨道全充满,G+中所有电子正好全部充满K、L、M三个电子层。M、N原子的价层电子构型为nS1,其电离能数据如下表:
| M | N | |
| 第一电离能(kJ/mol) | 495.8 | 418.8 |
回答下列问题:
(1)Z元素原子的价层电子的轨道表示式为: ;
(2)由X、Y形成的Y2X2分子中,含有 个![]() 键, 个
键, 个![]() 键:
键:
(3)比较ME、NE的熔点高低并说明理由 。
(4)Y、Z、Q的第一电离能由小到大的顺序为 。(用元素符号回答)
(5)YQ2中心原子的杂化方式为___________,有一种与YQ2互为等电子体的离子,能用于鉴别Fe3+ ,写出其电子式________________。
(6)GE的晶胞结构如图所示,阴离子周围最近的阳离子有 个;GE晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出计算式)。
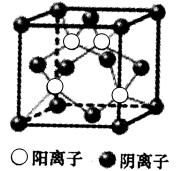
查看答案和解析>>
科目: 来源: 题型:
将等物质的量的X.Y气体充入一容积可变的密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)+2M(s)![]() 2Z(g);
2Z(g);![]() 。当改变某个条件并维持新条件直至达到新平衡,下表中关于新平衡与原平衡的比较,正确的是 ( )
。当改变某个条件并维持新条件直至达到新平衡,下表中关于新平衡与原平衡的比较,正确的是 ( )
| 改变的条件 | 正.逆反应速率变化 | 新平衡与原平衡比较 | |
| A | 升高温度 | 逆反应速率增大量大于正反应速率增大量 | X的体积分数增大 |
| B | 增大压强 | 正反应速率增大,逆反应速率减小 | Z的浓度不变 |
| C | 减小压强 | 正.逆反应速率都减小 | Y的体积分数变大 |
| D | 充入一定量的Z | 逆反应速率增大 | X的体积分数变大 |
查看答案和解析>>
科目: 来源: 题型:
黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如下图所示:

已知:①王水是由1体积的浓硝酸(ρ=1.42g·cm-3)和3体积的浓盐酸(ρ=1.19g·cm-3)混合而成的。
②黄铁矿和王水反应的方程式为FeS2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)简述实验室配制王水的操作过程_____________________________________
________________________________________________________________。
(2)方法一中过滤、洗涤、灼烧都用到的仪器是_______________。
(3)方法二中要判断BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是_________(填代号)
A.BaCl2 B.NaOH C.Na2SO4 D.HCl
(4)实验室利用下列装置和试剂制取少量氯化氢气体试剂:①浓硫酸 ②浓盐酸 ③食盐固体
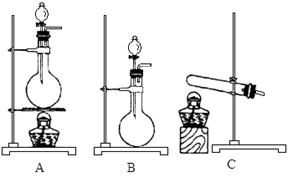
若选用试剂①③,则应选择的装置是___________(填代号,下同);推测发生反应的化学方程式为__________________________________________________;
若选用试剂①②,则宜选择的装置是____________。
(5)方法一中,灼烧时发生反应的化学反应方程式为________________________ ;已知称取黄铁矿样品的质量为1.50g,称得灼烧后固体的质量为0.8g,不考虑操作误差,则该矿石中FeS2的质量分数是________________。
查看答案和解析>>
科目: 来源: 题型:
下列取代基或微粒中,碳原子都满足最外层为8电子结构的是( )
A.乙基(—CH2CH3) B.碳正离子[(CH3)3C+]
C.碳化钙 (CaC2) D.碳烯 (:CH2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com