
科目: 来源: 题型:
镁是很活泼的金属,常用作脱硫剂、脱氧剂。在电子工业中用镁制取硅的反应为:2Mg+SiO2![]() 2MgO+Si,同时有副反应发生:2Mg+Si
2MgO+Si,同时有副反应发生:2Mg+Si![]() Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430
Mg2Si,Mg2Si遇盐酸迅速反应生成SiH4,SiH4在常温下是一种不稳定、易分解的气体(燃烧热约为1430![]() )。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:
)。如图是进行Mg与SiO2反应的实验装置,试回答下列问题:

(1)由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气。X气体应选用①CO2、②N2、③H2中的 。
(2)当接通电源引发反应后,切断电源,反应能继续进行,其原因是
。证明了反应物Mg与SiO2具有的总能量 (填“大于”、“小于”或“等于”)生成物MgO和Si具有的总能量。
(3)反应结束时,待冷却至常温后,关闭K,从分液漏斗中加入稀盐酸,可观察到导管口a处有闪亮的火星。据此现象可推知 在空气中能自燃。燃烧的热化学方程式为
,当产生等量的热量时,燃烧CH4和SiH4的物质的量之比为 (CH4的燃烧热是890![]() )
)
查看答案和解析>>
科目: 来源: 题型:
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1) CuSO4 +Na2CO3 主要: Cu2+ + CO32─ + H2O = Cu(OH)2↓ + CO2↑
次要:Cu2+ + CO32─= CuCO3↓(几乎不发生反应。下同)
(2) CuSO4 +Na2S 主要: Cu2+ + S2─ = CuS↓
次要: Cu2+ + S2─ + 2H2O = Cu(OH)2↓ + H2S↑
则下列几种物质的溶解度大小的比较中,正确的是( )
A.CuS <Cu(OH)2<CuCO3 B.CuS >Cu(OH)2>CuCO3
C.Cu(OH)2>CuCO3>CuS D.Cu(OH)2<CuCO3<CuS
查看答案和解析>>
科目: 来源: 题型:
下列有关物质分类或归纳的说法中,正确的一组是
①蔗糖和麦芽糖的化学式都可用C12H22O11表示,它们互为同分异构体
②聚乙烯、聚氯乙烯、纤维素都属于合成高分子
③明矾、石膏、冰醋酸、水都是电解质 ④盐酸、漂白粉、水玻璃都是混合物
⑤分馏、干馏、裂化都是化学变化 ⑥植物油、直馏汽油都可与溴水反应
A.①③⑤ B.②④⑥ C.①③④ D.②⑤⑥
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数的值,下列有关说法正确的是 ( )
A.常温常压下,22.4 L O2所含的氧分子数目为NA
B.共含NA个氢原子的H2和CH4的混合气体总物质的量为0.5 mol
C.18 g H2O中所含的质子数为10NA
D.2 L 0.1 mol/L Na2CO3溶液中所含Na+的数目为0.2NA
查看答案和解析>>
科目: 来源: 题型:
T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C物质的量变化如图(Ⅰ)所示;若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )
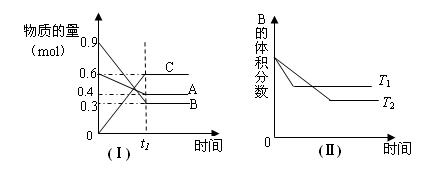
A.在(t1+1)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B.在(t1+1)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动
C.不再增减物质,只改变压强或温度时,A的体积分数V(A)%变化范围为25%<V(A)%<40%
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
查看答案和解析>>
科目: 来源: 题型:
某无色溶液可能含有Na+、Ba2+、NH4+、CO32-、SO32-、NO3-、SO42-、I-等离子。为鉴定这些离子,分别取少量溶液进行以下实验:
①取样品进行焰色实验,焰色呈黄色;
②取样品加BaCl2溶液,立即产生白色沉淀。过滤后,向白色沉淀中加入足量盐酸,沉淀部分溶解;
③取样品加入少量淀粉溶液,再加入过量氯水,无明显现象;
④取样品加入足量稀H2SO4,生成无色气体。该气体不能使澄清石灰水溶液变浑浊,但遇空气后立即变成红棕色;
分析上述4个实验,回答下列问题。
(1) 该溶液中肯定不含的离子是 ,不能确定的离子是 ;
(2) 写出第④步中加入稀H2SO4生成气体的离子方程式 ;
(3) 设计实验检验第(1)题中不能确定的离子:取样品于试管中,
,则说明含有该离子。
查看答案和解析>>
科目: 来源: 题型:
下列实验设计及其对应的离子方程式均正确的是
A. 钠与水反应:Na+2H2O=Na++2OH-+H2↑
B. 用过氧化钠与水反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑
C. 用氨水检验氯化镁溶液中混有氯化铝杂质:
Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D. 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是:( )(用NA代表阿伏加德罗常数的值)
A、标准状况下,5.6L一氧化氮和5.6L氧气混合后的气体中分子总数为0.5NA
B、2.7g金属铝变为铝离子时失去的电子数为0.3NA
C、在标准状况下,体积均为22.4L的CH4与H2O所含有的电子数均为10NA
D、CO和N2为等电子体,22.4L的CO气体与1molN2所含的电子数相等
查看答案和解析>>
科目: 来源: 题型:
下列各组元素性质递变错误的是
A.Li、Be、B原子最外层电子数逐渐增多 B.N、O、F氢化物的稳定性依次减弱
C.P、S、Cl最高正价依次升高 D.Li、Na、K的金属性依次增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com