
科目: 来源: 题型:
下列有关有机物的说法不正确的是 ( )
A.酒精中是否含有水,可用金属钠检验
B.有机酸和醇脱水合成的某些酯,可用作糖果、化妆品中的香料
C.蛋白质在一定条件下能发生水解反应,生成氨基酸
D.乙烯通过聚合反应可合成聚乙烯,聚乙烯塑料可用来制造多种包装材料
查看答案和解析>>
科目: 来源: 题型:
NA表示阿伏加德罗常数,下列叙述正确的是
A.2mol NO2与水反应转移电子数为NA
B.1.7gH2O2中含的电子数为0.9NA
C.1mol甲烷中的氢原子被氯原子完全取代,需要氯气分子数为2NA
D.pH=13的NaOH溶液含OH-的数目为0.1 NA
查看答案和解析>>
科目: 来源: 题型:
下列实验操作,正确的是
A.中和滴定时,用标准液润洗滴定管,用待测液润洗锥形瓶,并滴入l mL指示剂
B.配制物质的量浓度溶液时,将称量好的溶质溶于盛有适量水的烧杯中,溶解后立即倾入容量瓶中,继续进行洗涤和定容
C.制取Fe(OH)2时,吸取NaOH溶液的胶头滴管的末端应插入FeSO4溶液中,再缓缓将NaOH溶液挤出
D.溴乙烷和烧碱溶液共热后,将硝酸银溶液滴入水解液中,即可见到淡黄色沉淀
查看答案和解析>>
科目: 来源: 题型:
某原电池的电池反应为:Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是
A.铜片、铁片、FeCl3溶液组成的原电池
B.石墨、铁片、Fe(NO3)3溶液组成的原电池
C.铁片、锌片、Fe2(SO4)3溶液组成的原电池
D.银片、铁片、Fe(NO3)2溶液组成的原电池
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D是短周期元素形成的四种气体单质。E、F均为气体,且F为
红棕色。有关的转化关系如下图所示(反应条件均已略去)。
请回答下列问题:
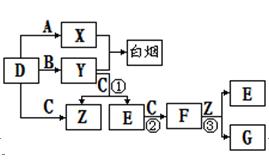
(1)D的化学式为 ;
(2)反应③的离子方程式为 。
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为 。
(4)0.1mol/L的X溶液和0.1mol/L的Y溶液等体积混合,溶液呈________性;(填“酸”、“碱”或“中”)原因是: __________________________________
(用离子方程式说明)
(5)常温下0.1mol/L的Y溶液中c(H+)/c(OH-)=1×10-8,下列叙述正确的是( )
A.该溶液的pH=11;
B.该溶液中的溶质电离出的阳离子浓度0.1mol/L
C.该溶液中水电离出的c(H+)与c(OH-)乘积为1×10-22
D.pH=3的盐酸溶液V1 L与该0.1mol/L的Y溶液V2 L混合,若混合溶液pH=7,则:V1>V2
E.将以上溶液加水稀释100倍后,pH值为9;
查看答案和解析>>
科目: 来源: 题型:
有一硝酸盐晶体,其化学式为M(NO3)x·yH2O,相对分子质量为242。取1.21g该晶体溶于水,配成100mL溶液,将此溶液用石墨作电极进行电解,当有0.01mol电子发生转移时,溶液中金属全部析出。经称量阴极增重0.32g。求:
(1)金属M的相对原子质量及x、y值。
(2)电解后溶液的pH(电解过程中溶液体积变化忽略不计)。
查看答案和解析>>
科目: 来源: 题型:阅读理解
据报道双氧水接触银能剧烈反应,为消除用硝酸清洗试管内壁上的银时产生的有毒气体污染环境,体现“绿色化学”的理念,某学校活动小组利用该反应清洗试管内壁上的银,并进一步研究反应的机理。他们查阅资料(资料信息:硝酸氧化性比过氧化氢强,能氧化过氧化氢;碘化银为黄色固体;稀硝酸与银单质反应条件为加热),设计并完成了以下实验。
第一步 清洗: 取10 mL 10% H2O2溶液清洗附有银的试管。反应剧烈,并产生大量的气体(经验证为氧气),试管内壁上的银全部被清除干净,最后得澄清透明液体a。用激光照射液体a能看到丁达尔效应。
第二步 探究反应原理: 取2支试管,分别取液体a约1 mL,稀释至3 mL得液体b。
学生甲:将1支盛有液体b的试管进行如下实验

学生乙:向液体b中加入4~5滴稀硝酸酸化的2 mol/LNaCl溶液,溶液中出现白色沉淀。
通过上述实验,他们认为H2O2氧化了银单质。请回答:
(1)液体a在分散系分类中属于 。
(2)操作x名称是 。
(3)学生甲在液体b中加入碘化钾溶液,没有看到预期的黄色的碘化银沉淀,可能的原因是 (填序号)。
①液体a中的银元素大多数以银单质的形式存在
②过量的H2O2将I—氧化为I2
③加入的碘化钾溶液量太少
(4)学生乙在实验中加入4~5滴稀硝酸酸化的原因是 。
(5)如果银与H2O2反应生成的物质对H2O2的分解有催化作用,通过分析可以推测,起催化作用的物质是
查看答案和解析>>
科目: 来源: 题型:
下列溶液中,有关离子一定能大量共存的是( )
A.能使石蕊呈红色的溶液中: Na+、I-、Cl-、NO3-
B.能使甲基橙呈黄色的溶液中:K+、SO32-、SO42-、ClO-
C.能使pH试纸变红色的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+
D.无色溶液中:K+、Cl-、NO![]() 、SO
、SO![]()
查看答案和解析>>
科目: 来源: 题型:
已知下列元素的半径为:
| 原子 | N | S | O | Si |
| 半径r/ | 0.75 | 1.02 | 0.74 | 1.17 |
根据以上数据,磷原子的半径可能是
A.0.80×![]() B.1.10×
B.1.10×![]()
C.1.20×![]() D.0.70×
D.0.70×![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com