
科目: 来源: 题型:
四种短周期元素的性质或结构信息如下表。请根据信息回答下列问题。
| 元素 | A | B | C | D |
| 性质 结构 信息 | 室温下单质呈粉末状固体,加热易熔化。 单质在空气中燃烧,发出明亮的蓝紫色火焰。 | 单质常温、常压下是气体,能溶于水。 原子的M层有1个未成对的p电子。 | 单质质软、银白色固体、导电性强。 单质在空气中燃烧发出黄色的火焰。 | 原子最外层电子层上s电子数等于p电子数。 单质为空间网状晶体,具有很高的熔、沸点。 |
⑴B元素在周期表中的位置 ,写出A原子的电子排布式 。
⑵写出C单质与水反应的化学方程式 。
⑶D元素最高价氧化物晶体的硬度 (填“大 ”或“小”),其理由是 。
⑷A、B两元素非金属性较强的是(写元素符号) 。写出证明这一结论的一个实验事实 。
查看答案和解析>>
科目: 来源: 题型:
物质A~G均由短周期元素组成,A、B为非金属气体单质,B原子最外层电子数比次外层电子数的2倍还多1。甲、乙均为金属单质,且甲的原子半径在第三周期最大。各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):
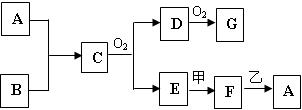
请回答:
(1)物质D的化学式 ;
(2) 物质A的电子式是 ;
(3)实验室制取C的化学方程式 ;
(4)物质F和乙反应生成A的离子方程式 。
查看答案和解析>>
科目: 来源: 题型:
离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO3-的摩尔电导率分别为0.60、1.98、0.45,据此可判断,往饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是 ( )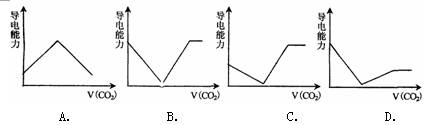
查看答案和解析>>
科目: 来源: 题型:
向MgSO4和Al2(SO4)3的混合溶液中, 逐滴加入NaOH溶液。下列图象中, 能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积, 纵坐标表示反应生成沉淀的质量)
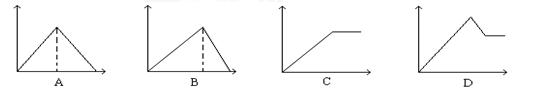
查看答案和解析>>
科目: 来源: 题型:
(1)49 g硫酸的物质的量为 mol,若在水中完全电离可产生 molH+ , ______mol![]() .若有一定量的硫酸完全电离产生
.若有一定量的硫酸完全电离产生![]() 个
个![]() ,此硫酸的质量为 _______g.
,此硫酸的质量为 _______g.
(2)标准状况下,11.2L的H2S气体质量为17g,则H2S的摩尔质量是 ,相对分子质量为 ; 同温同压下NH3与H2S密度之比为 ; 1.7g氨气与 mol H2O含有的电子数相等。
查看答案和解析>>
科目: 来源: 题型:
某溶液中有NH4+、Mg2+、Fe2+和Fe3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
A. NH4+ B. Fe2+ C. Mg2+ D. Fe3+
查看答案和解析>>
科目: 来源: 题型:
目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
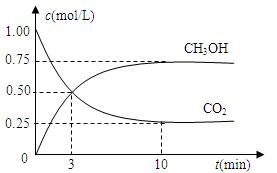
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)。
(2)该反应的平衡常数表达式为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1 mol CO2和4 mol H2
(4)如果在相同的容器中事先充入1 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为 。
查看答案和解析>>
科目: 来源: 题型:
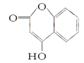 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
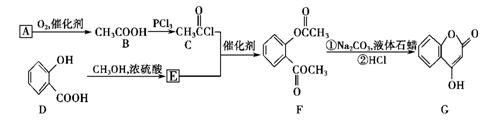
(1)A与银氨溶液反应有银镜生成,则A的结构简式是________。
(2)B―→C的反应类型是________。
(3)E的结构简式是________。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:_________________________。
(5)下列关于G的说法正确的是________。
a.能与溴单质反应 b.能与金属钠反应
c.1 mol G最多能和3 mol氢气反应 d.分子式是C9H6O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com