
科目: 来源: 题型:
利用碳棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当碳棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗。试计算:
(1)锌片的质量减少了多少?
(2)原稀硫酸溶液的物质的量浓度。
(3)有多少个电子通过了导线。
查看答案和解析>>
科目: 来源: 题型:
锌和足量的稀HCl反应时,加入少量CuSO4固体,下列叙述正确的是:
A.反应速率减慢,产生H2的量不变
B.反应速率加快,产生H2的量不变
C.反应速率不变,产生H2的量增加
D.反应速率加快,产生H2的量减少
查看答案和解析>>
科目: 来源: 题型:
氯气溶于水即得氯水,下列关于氯水的叙述,正确的是( )
A.新制的氯水中只含Cl2和H2O两种分子
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是Cl2
D.氯水在密封无色玻璃瓶中放置数天后酸性将减弱
查看答案和解析>>
科目: 来源: 题型:
根据元素周期表的结构,回答下面两个小题。
(1)A、B、C、D、X五种元素在周期表中的位置如图所示(X与A、B为相邻族,与C、D为相邻周期),若元素X的原k*s^5#u子序数为x,则A、B、C、D四种元素的原k*s^5#u子序数之和为 或 (用含x的代数式表示)。

(2)在下列各元素组中,除一种元素外,其余都可以按照某种共性归属一类,请选出各组的例外元素,并将该组其他元素的可能归属按所给六种类型的编号填入表内。
| 元素组 | 例外元素 | 其他元素所属编号 |
| (a)S、Na、Mg、N | ||
| (b)N、P、Sn、As | ||
| (c)K、Ca、Al、Zn | ||
| (d)Cu、Fe、Ag、Ca |
其他元素所属类型编号:①主族元素,②过渡元素,③同周期元素,④同主族元素,⑤金属元素,⑥非金属元素。
查看答案和解析>>
科目: 来源: 题型:

a.相同条件下卤化银的Ksp按AgCl、AgBr、AgI 的顺序依次增大
b.卤化氢溶入水的酸性按HF、HCl、HBr、HI的顺序依次减弱
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质氧化性按F2、Cl2、Br2、I2的顺序依次减弱
(6)卤化氢的键能与键长大小如下表。
| HF | HCl | HBr | HI | |
| 键能/kJ·mol-1 | 568.6 | 431.8 | 365.7 | 298.7 |
| 键长/pm | 92 | 127.6 | 141.0 | 162 |
由上表数据可以推断:
①卤素单质非金属性越强,与氢化合生成的氢化物越 (填“稳定”或“不稳定”)。
②卤化氢的键长与卤离子的半径的关系是: 。
查看答案和解析>>
科目: 来源: 题型:
有机物甲的分子式为 CxHyO2, 其中O%为20.25%,C%为68.35%。在酸性条件下,甲水解为乙和丙两种有机物,在相同温度和压强下,同质量的乙和丙的蒸气所占的体积相同,则甲的可能结构有 ( )。
A.8 种 B.14种 C.16种 D.18种
查看答案和解析>>
科目: 来源: 题型:
有常见A、B、C三种短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素最外层电子数比B多一个;甲、乙、丙是三种含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙溶液pH>7,乙溶液pH<7,丁为气体,戊为淡黄色固体,甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如下图:
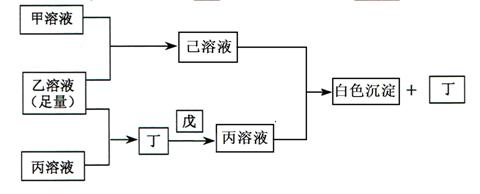
请回答:
(1)写出C元素的原子结构示意图__________________________。
写出丁和戊的电子式:__________________________。
(2)用有关化学用语解释乙溶液呈酸性的原因:__________________________。
丙溶液呈碱性的原因:_______________________________________。
(3)写出有关反应的离子方程式:_____________________________。
①乙溶液+丙溶液→丁:_____________________________________________。
②己溶液+丙溶液→丁:_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
用![]() 表示阿伏加德罗常数的值。下列叙述正确的是( )
表示阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,1L辛烷完全燃烧后,所生成气态产物的分子数为![]()
B.常温常压下,每生成![]() 时转移的电子数为
时转移的电子数为![]()
C.常温常压下,46g二氧化氮和四氧化二氮混合物中含![]() 个原子
个原子
D.1mol含5个碳原子的有机物,最多形成碳碳单键数为![]()
查看答案和解析>>
科目: 来源: 题型:
一定温度下,某密闭容器里发生如下反应:CO(g)+H2O![]() CO2(g)+H2(g)(正反应为吸热反应),当反应达到平衡时,测得容器中各物质的物质的量均为1 mol。欲使
CO2(g)+H2(g)(正反应为吸热反应),当反应达到平衡时,测得容器中各物质的物质的量均为1 mol。欲使![]() 的物质的量浓度增大1倍,在其他条件不变时,下列措施中可采用的是
的物质的量浓度增大1倍,在其他条件不变时,下列措施中可采用的是
①升高温度 ②增大压强 ③再通入1 mol![]() 和1 mol
和1 mol![]() ④再通入2 mol CO和2 mol
④再通入2 mol CO和2 mol![]()
A.①② B.②④ C.③④ D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com