
科目: 来源: 题型:
乙醇催化氧化为乙醛过程中化学键的断裂与形成情况可表示如下:
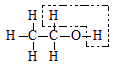
![]()
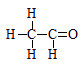 (注:含-CHO的物质为醛类化合物)
(注:含-CHO的物质为醛类化合物)
下列醇不能被氧化为醛类化合物的是 ( )
A.CH3OH B.![]()
C.![]() D.CH3CH2CH2OH
D.CH3CH2CH2OH
查看答案和解析>>
科目: 来源: 题型:
下列说法错误的是 ( )
①化学性质相似的有机物是同系物
②分子组成相差一个或n个“CH2”原子团的有机物是同系物
③若烃中碳、氢元素的质量分数相同,它们必定是同系物
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似
A.①②③④ B.只有②③ C.只有③④ D.只有①②③
查看答案和解析>>
科目: 来源: 题型:
氮化钠和氢化钙都是离子化合物,与水反应的化学方程式(未配平)如下:
Na3N+H2O →NaOH +NH3 ,CaH2+H2O →Ca(OH)2 +H2.有关它们的叙述:
①离子半径:Na+>N3->H+ ;②与水反应都是氧化还原反应;③与水反应后的溶液都显碱性;④与盐酸反应都只生成一种盐;⑤两种化合物中的阴阳离子均具有相同的电子层结构。其中正确的是 ( )
A.②③④⑤ B.①③⑤ C.②④ D.③
查看答案和解析>>
科目: 来源: 题型:
如右图为元素F、S、Cl在周期表中的位置,关于F、S、Cl的说法正确的是
A.非金属性:F > S > Cl B.原子半径:Cl > S > F
C.稳定性:HF > HCl > H2S D.酸性:HClO4 > H2SO4
| He | ||
| F | ||
| S | Cl | |
查看答案和解析>>
科目: 来源: 题型:
已知AgI胶体粒子能吸附I-,在10 mL 0.01 mol· L-1 KI溶液中滴入8~10滴0.01 mol· L-1 AgNO3溶液后,将溶液装入半透膜袋中,并浸没在蒸馏水中,隔一段时间后,水中含有的离子最多的是( )
A.H+、OH- B.K+ 、I- C.Ag+、NO3- D.K+
查看答案和解析>>
科目: 来源: 题型:
关于实验下列说法错误的是( )
A.在硫酸铜晶体结晶水含量的测定实验中,加热后的硫酸铜应在空气中冷却后再称量
B.在中和热的测定实验中,应用稀的强酸和强碱作为反应物进行实验 [
C.在Fe(OH)3胶体的电泳实验中,靠近阴极附近的液体的颜色会加深
D.在硫酸铜晶体结晶水含量的测定实验中,加热不够充分将会使实验结果偏小
查看答案和解析>>
科目: 来源: 题型:
锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量占世界第一。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:
2Sb2S3+3O2+6Fe=Sb4O6+6FeS ……………①
Sb4O6+6C=4Sb+6CO ………………………②
关于反应①、反应②的说法正确的是
A. 反应①②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3 mol FeS时,共转移6 mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成4 mol Sb时,反应①与反应②中还原剂的物质的量之比为4︰3
查看答案和解析>>
科目: 来源: 题型:
![]() 肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。
肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料。
(1)已知:N2(g)+2O2(g)=2NO2(g) △H= +67.7 kJ/mol
2N2H4(l)+2NO2(g)=3N2(g)+4H2O(g) △H= -1135.7 kJ/mol
则肼完全燃烧的热化学方程式为______________________________________________。
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%—30%的KOH溶液。该电池放电时,正极的电极反应式是______________________________________,电池工作一段时间后,电解质溶液的pH将_________(填“增大”、“减小”、“不变”)。
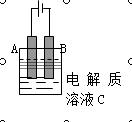
(3)上图是一个电化学装置示意图。用肼——空气燃料电池做此装置的电源。如果A是铂电极,B是石墨电极,C是AgNO3溶液, 若B极增重10.8 g,该燃料电池理论上消耗_____mol N2H4。
(4)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示
肼的水溶液显碱性的原因_________________________________。
查看答案和解析>>
科目: 来源: 题型:
油脂是油与脂肪的总称,它是多种高级脂肪酸的甘油酯。油脂既是重要食物,又是重要的化工原料。油脂的以下性质和用途与其含有的不饱和双键(C=C)有关的是( )[
A.适量摄入油脂,有助于人体吸收多种脂溶性维生素和胡萝卜素
B.利用油脂在碱性条件下的水解,可以生产甘油和肥皂
C.植物油通过氢化可以制造人造奶油
D.脂肪是有机体组织里储存能量的重要物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com