
科目: 来源: 题型:
FeCl2溶液中混有FeI2杂质,根据已知反应:①2FeCl3+2KI=2FeCl2+2KCl+I2;②2FeCl2+Cl2=2FeCl3;③F2+2KI(固)=2KF+I2中的有关事实,要除去其中的FeI2,应选用的试剂是
A.F2 B.过量Cl2 C.FeCl3 D.FeCl2
查看答案和解析>>
科目: 来源: 题型:
有A、B、C、D、E五种烃,具有下列性质:①各取0.1mol分别充分燃烧,其中B、C、E燃烧所得的CO2均为4.48L(标准状况),A和D燃烧所得的CO2都是前三者的3倍;②在适宜条件下,A、B、C都能跟氢气发生加成反应,其中A可以转化为D、B可以转化为C,C可以转化为E;③B和C都能使溴水或酸性KmnO4溶液褪色,而A、D、E无此性质;④用铁屑作催化剂时,A可与溴发生取代反应。判断A、B、C、D、E各是什么物质,写出结构简式.
A_________B__________C__________D___________E_______。
查看答案和解析>>
科目: 来源: 题型:
吗啡和海洛因都是严格查禁的毒品。吗啡分子中C、H、N、O的质量分数分别为71.58%、6.67%、4.91%和16.84%。已知其相对分子质量不超过300
(1)求吗啡的分子式(要有计算步骤)
(2)已知海洛因是吗啡的二乙酸酯,求海洛因的摩尔质量。(只填结果)
查看答案和解析>>
科目: 来源: 题型:
(5分)有5种烃:甲烷、乙炔、苯、环己烷、甲苯,分别取一定量的这些烃,完全燃烧后生成m mol CO2和n mol H2O。则
(1) 当m=n时,该烃是
(2) 当m=2n时,该烃是
(3) 当2m=n时,该烃是
(4) 当4m=7n时,该烃是
查看答案和解析>>
科目: 来源: 题型:
若X、Y两种元素在周期表中位于同一主族,且相隔一个周期,并有m=n>0。在一定条件下有下列反应(未配平):Xm + Yn + H2O → HXO3 + HY。请回答:
⑴该反应的还原剂的电子式为___________________。
⑵配平上述化学方程式(用化学式表示):
⑶若某化学反应如下:(未配平)KX + Yn + H2O → KXO3 + Xm + HY + KY
若KXO3和Xm的化学计量数均为1,则Yn的化学计量数为____________。
在下面化学式上标出电子转移的方向和数目:
KX + Yn + H2O →
⑷已知:在反应中,若氧化反应和还原反应发生在同一分子内部处于同一化合价的同种元素上,使该元素的原子(或离子)一部分被氧化,另一部分被还原。这种自身的氧化还原反应称为歧化反应。实验室模拟KXO3的制法如下:
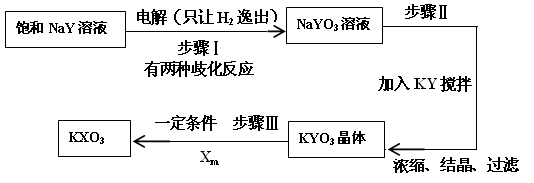
①在进行步骤Ⅰ实验时,有学生主张电解装置用U形管,有的学生主张用烧杯,你认为用哪种仪器更合适______________(填名称)。
②步骤Ⅰ的阴极电极反应式为(用化学式表示):_____________________。
③步骤Ⅰ中生成NaYO3的歧化反应的离子方程式为(用化学式表示):______________________。
④步骤Ⅱ中向NaYO3的溶液中加入粉末状的KY,搅拌后生成KYO3。已知有2L 3 mol·L-1的NaYO3溶液,则至少需要加入__________mol KY粉末可将溶液中的YO3-离子沉淀至浓度变为0.1 mol·L-1。[已知Ksp(KYO3)= 0.366,计算结果保留两位小数,加入KY粉末后溶液体积不变]
查看答案和解析>>
科目: 来源: 题型:
工业上生产MnO2和Zn的主要反应有:
①MnO2(矿石)+ZnS+2H2S4=MnSO4+ZnSO4+S+2H2O
②MnSO4+ZnSO4+2H2O![]() MnO2+Zn+2H2SO4 下列说法正确的是
MnO2+Zn+2H2SO4 下列说法正确的是
A.①中MnO2和H2SO4都是氧化剂 B.①中析出32gS时转移1mol电子
C.②中MnSO4发生氧化反应 D.②中生成的Zn在阳极析出
查看答案和解析>>
科目: 来源: 题型:
I.恒温、恒压下,在一个可变容积的容器中发生如下发应:A(g)+B(g)![]() C(g)
C(g)
(1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时A的物质的量为 mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为 mol。
(3)若开始时放入x m![]() olA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3a mol,则x= mol,y= mol。平衡时,B的物质的量 (选填一个编号)(甲)大于2 mol (乙)等于2 mol(丙)小于2 mol (丁)可能大于、于或小于2mol作出此判断的理由是 。
olA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3a mol,则x= mol,y= mol。平衡时,B的物质的量 (选填一个编号)(甲)大于2 mol (乙)等于2 mol(丙)小于2 mol (丁)可能大于、于或小于2mol作出此判断的理由是 。
(4)若在(3)的平衡混合物中再![]() 加入3molC,待再次到达平衡后,C的物质的量分数是 。
加入3molC,待再次到达平衡后,C的物质的量分数是 。
II.若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(5)开始时放入1molA和1molB到达平衡后生成b molC。将b与(1)小题中的a进行比较 (选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是 。
查看答案和解析>>
科目: 来源: 题型:
M、N、R、T为周期表中前四周期相邻两个周期的元素,且原子序数依次增大。已知T的次外层上电子没有排满,且该能层中成对电子数等于其它各能层上电子的总数;R和T在同一族;N的外围电子总数为6,均为未成对电子。根据以上信息,回答下列问题:
(1)T的元素符号为 ,在周期表中位于 族,N的价电子排布式为 。
(2)M和R两种元素组成的常见化合物有两种,其中一种可以单质之间进行化合,生成R的高价态化合物,请写出该反应的化学方程式: 。
(3)表面上附着氮原子的R可做为工业催化剂,下图为氮原子在R的晶面上的单层附着局部示意图(图中小黑色球代表氮原子, 灰色球代表R原子)。则图示颗粒表面上氮原子与R原子的个数比为 。

(4)T、N都有多种配合物,[T(NH3)3(H2O)M2]M是T配合物的一种,其中心离子的化合价为 ,配位数为 。N与甲基丙烯酸根的配合物为:
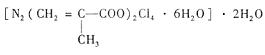 该化合物中存在的化学键类型有 。甲基丙烯酸分子中C原子的杂化方式有 。
该化合物中存在的化学键类型有 。甲基丙烯酸分子中C原子的杂化方式有 。
查看答案和解析>>
科目: 来源: 题型:
在pH=1的溶液中能大量共存的一组离子或分子是
A. Na+、Mg2+、ClO—、NO3— B. Al3+、 NH4+、 Br- 、Cl-
C. K+ 、Cr2O72- 、CH3CHO、 SO42- D. Na+、K+ 、SiO32-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com