
科目: 来源: 题型:
从含铜、银、金和铂的块状金属废料中提取铂、金、银的一种工艺如下:
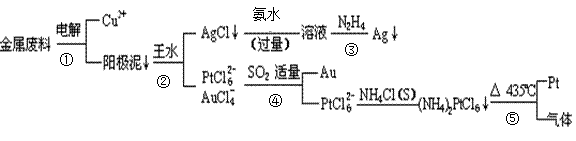
根据以上工艺回答下列问题:
(1)电解时,以_____________为阳极,纯铜为阴极,CuSO4溶液为电解液,则阴极的电极反应方程式为
(2)AgCl溶于氨水后所得的溶液含有的一种阳离子,在碱性条件下,也可用葡萄糖将其还原为银,写出该反应的离子方程式:
(3)写出步骤④的离子方程式:
(4)金和浓硝酸反应的化学方程式为:Au +6HNO3(浓)![]() Au(NO3)3+3NO2↑+ 3H2O,因该反应正向进行的程度极小,所以金几乎不溶于浓硝酸,但金却可以溶于王水,试简要解释之:
Au(NO3)3+3NO2↑+ 3H2O,因该反应正向进行的程度极小,所以金几乎不溶于浓硝酸,但金却可以溶于王水,试简要解释之:
(5)写出反应⑤的化学反应方程式
____________________________________________________________________________
查看答案和解析>>
科目: 来源: 题型:
已知空气—锌电池的电极反应为
锌片:Zn+2OH――2e-=ZnO+H2O;
碳棒:O2+2H2O+4e- =4OH- ,据此判断,锌片是( )
A.正极,被还原 B.正极,被氧化C.负极,被还原 D.负极,被氧化
查看答案和解析>>
科目: 来源: 题型:
4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1∶2,X2+ 和Z-离子的电子数之差为8。下列说法不正确的是 ( )
A.与W相邻的同主族元素形成的单质晶体中原子个数与共价键数之比为1︰4
B.元素原子半径从大到小的顺序是X、Y、Z
C.WZ4分子中W、Z原子通过共价键结合且最外层均达到8电子结构
D.W、Y、Z元素最高价氧化物对应的水化物中酸性最强的元素是Z
查看答案和解析>>
科目: 来源: 题型:
在碱存在的条件下,卤代烃与醇反应生成醚(R-O-R′):
![]()
化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下:
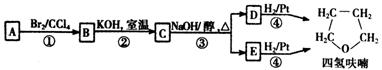
请回答下列问题:
(1)1 mol A和1 mol H2在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数约为65%,则Y的分子式为 __________________________
A分子中所含官能团的名称是 __________________________
A的结构简式为__________________________。
(2)第①②步反应类型分别为① _____________ ② _____________。
(3)化合物B具有的化学性质(填写字母代号)是 _____________。
a.可发生氧化反应 b.强酸或强碱条件下均可发生消去反应
c.可发生加成反应 d.催化条件下可发生加聚反应
(4)写出C、D和E的结构简式:
C _____________ D ___________________E_____________
(5)写出化合物C与NaOH水溶液反应的化学方程式:
_____________________________________________________________________________
(6)写出四氢呋喃链状醚类的所有同分异构体的结构简式:
_____________________________________________________________________________
____________________________________________________________________________
查看答案和解析>>
科目: 来源: 题型:
现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是
A.(1-a)/7 B.3a/4 C.6(1-a)/7 D.12(1-a)/13
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.电离平衡常数受溶液浓度的影响
B.电离平衡常数可以表示弱电解质的相对强弱
C.电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大
D.H2CO3的电离常数表达式:K=
查看答案和解析>>
科目: 来源: 题型:
NA代表阿伏加德罗常数,下列说法正确的是 ( )
A.23gNa在空气中加热完全变成Na2O2时失去2NA个电子
B.标准状况下,22.4LH2含有NA个H2分子
C.1mol/L的硝酸钠溶液中含有的硝酸根离子数为NA
D.0.5molKClO3中含有ClO3-的数目为NA
查看答案和解析>>
科目: 来源: 题型:
在Cu2S+2Cu2O=6Cu+SO2↑反应中,说法正确的是
A.Cu2S在反应中既是氧化剂,又是还原剂
B.Cu是氧化产物
C.氧化剂只有Cu2O
D.生成1mol Cu,反应中转移2mol电子
查看答案和解析>>
科目: 来源: 题型:
在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。该氧化物又可以经过此反应的逆反应,生成颗粒很细的铁粉。这种铁粉具有很高的反应活性,在空气中受撞击或受热时会燃烧,所以俗称“引火铁”。请分别用下图中示意的两套仪器装置,制取上述铁的氧化物和“引火铁”。实验中必须使用普通铁粉和6mol/L盐酸,其他试剂自选(装置中必要的铁架台、铁夹、铁圈、石棉网、加热设备等在图中均已略去).
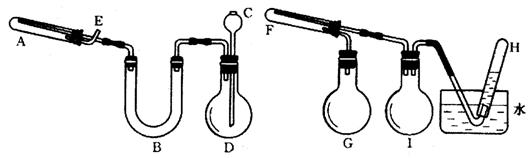
填写下列空白:
(1)长颈漏斗C中应加入___________;实验时,U型管B中应加入的试剂是_______。烧瓶D中发生的反应有时要加入少量硫酸铜溶液,其目的是_________________ 。
(2)试管F中发生反应的化学方程式是______________________________。
(3)实验进行时,烧瓶G的作用是__________________________;
烧瓶I的作用是___________________________。
(4)在A、D、F、G、I各仪器中,在实验时不需要加热的仪器是(填该仪器对应的字母)_____________。
(5)为了安全,在A管中的反应发生前,在E出口处必须_____________;A管中的反应开始后,在E出口处应 ___________________________。
查看答案和解析>>
科目: 来源: 题型:
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
A.4 g重水(D2O)中所含质子数为0.2×6.02×1023
B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2×6.02×1023
C.4.48 L H2和O2的混合气体中所含分子数为0.2×6.02×1023
D.0.1 mol Cl2溶解于NaOH溶液中,转移电子数为0.2×6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com