
科目: 来源: 题型:
下列各离子组,能够在同一溶液中大量共存的是 ( )
A.NH4+、K+、CO32—、OH— B.Ba2+、Na+、SO42—、NO3—
C.Na+、Ag+、HCO3—、I— D.K+、NH4+、Cl—、Br—
查看答案和解析>>
科目: 来源: 题型:
利用下列反应:Fe+Cu2+===Fe2++Cu设计一个化学电池(给出若干导线和一个小灯泡,电极材料和电解质溶液自选),画出实验装置图,注明电解质溶液的名称和正负极材料,标出电子流动方向和电流方向,写出电极反应式。
查看答案和解析>>
科目: 来源: 题型:
氢—氧燃料电池是将H2和O2分别通入电池,穿过浸入20%~40%的KOH溶液的多孔碳电极,其电极反应式为:2H2+4OH--4e-===4H2O和O2+2H2O+4e-===4OH- 。则下列叙述正确的是:
通H2的一极是正极,通O2的一极是负极?
通O2的一极是正极,通H2的一极是负极
C. 工作一段时间后电解质溶液pH增大?
D. 工作时正极区附近pH减小?
查看答案和解析>>
科目: 来源: 题型:
哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充人1mol N2和3mol H2,在一定条件下使该反应发生:N2+3H2![]() 2NH3。下列有关说法正确的是( )
2NH3。下列有关说法正确的是( )
A.达到化学平衡时,正反应和逆反应的速率都为零
B.当符合:3u正(N2)=u正(H2)时,反应达到平衡状态
C.达到化学平衡时,单位时间消耗amolN2,同时生成3amolH2
D.当N2、H2、NH3的分k*s^5#u子数比为1∶3∶2,反应达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
下列对于硫酸、硝酸的认识,正确的是( )
A. 浓硫酸和浓硝酸都具有氧化性 B. 铜和浓硫酸的反应属于置换反应
C. 在铜和浓硝酸的反应中,硝酸只发挥了氧化性,没有体现酸性
D. 可用铝或铁制容器盛装稀硝酸
查看答案和解析>>
科目: 来源: 题型:
已知:以铜作催化剂,用空气氧化醇制取醛,事实上是空气先与铜反应生成氧化铜,热的氧化铜再氧化醇生成醛。某实验室中用甲醇、水、空气和铜粉(或氧化铜)制取甲醛溶液。下表给出甲醇、甲醛的沸点和水溶性:
| 沸点/℃ | 水溶性 | |
| 甲醇 | 65 | 与水混溶 |
| 甲醛 | -21 | 与水混溶 |
下图是两个同学设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,分别如甲和乙所示

请回答下列问题:
(1)在仪器组装完成后,加装试剂前必须要进行的操作是____________________。
(2)若按甲装置进行实验,则通入A的X是______,B中发生反应的化学方程式为_____________________。(有机分k*s^5#u子用结构式表示)
(3)若按乙装置进行实验,则B管中应装入的物质是__________。
(4)试管C中应装入的试剂是__________。
(5)两套装置中都需要加热的仪器有______(填A、B、C)。
(6)若欲得到较浓的甲醛溶液,你认为选用哪套装置较好?______(填“甲”或“乙”)。
(7)验证实验后试管C中含有甲醛,所用试剂是__________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
锂电池技术是新能源汽车的核心技术。下面是锂电池工作原理示意图:

左边是橄榄石结构的LiFePO4作为电池的正极,由铝箔与电池正极连接,中间是聚合物的隔膜,它把正极与负极隔开,Li+可以自由通过而 电子e-不能通过,右边是由石墨和Li组成的电池负极,由铜箔与电池的负极连接。电池的上下端之间是电池的电解质,电解质通常是LiClO4、LiAlCl4、LiAsF4等锂盐,溶剂通常用环脂、直链脂及酰胺等有机溶剂和一些非水无机溶剂。电池由金属外壳密闭封装。
请回答下列问题:
(1)锂电池比容量特别大的原因是: 。
(2)锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液?请用化学方程式表示其原因: 。
(3)某锂电池的电池反应方程式是Li+MnO2=LiMnO2。下列有关说法错误的是_________(填字母,下同)。
A.它的负极是锂
B.MnO2在电极反应中被还原
C.当有3.01×1023 个电子转移时,正极消耗1mol MnO2
D.配制锂电池中的电解质溶液可用直链脂等有机物作溶剂
(4)另有一种锂电池是将四氯铝锂溶解在亚硫酰氯(SOCl2)中作电解质溶液,电池总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S
已知亚硫酰氯和AlCl3??6H2O混合共热蒸干,可制得无水氯化铝AlCl3,则下列叙述正确的是____________。
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,SOCl2被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出的S的物质的量之比为4:1
查看答案和解析>>
科目: 来源: 题型:
据南京日报2009年11月9日报道,南京的空气质量拉响警报,8日全市污染指数更是超过300,达到重度污染,二氧化硫等污染物的浓度比平时高出2倍之多,秸秆焚烧再度成为城市空气急速污染的“元凶”。关于空气污染,下列说法正确的是( )
A.二氧化硫、二氧化氮、一氧化碳和二氧化碳是空气质量报告中涉及的主要污染物
B.正常雨水的pH等于7
C.二氧化硫和二氧化氮是引起酸雨的主要气体
D.秸秆焚烧总体来说对庄稼是有益的,值得提倡
查看答案和解析>>
科目: 来源: 题型:
A是生产某新型工程塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图所示(图中球与球之间连线代表化学键单键或双键)。
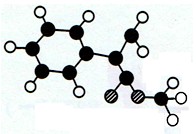
(1)根据分子结构模型写出A的结构简式______________________________。
(2)A在酸性条件下水解生成有机物B和甲醇,与B互为同分异构体的C:含苯环,能发生银镜反应,且苯环上只有一个支链。则C的结构简式为(写二种)_______________、_______________。
(3)拟以芳香烃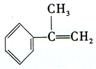 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:
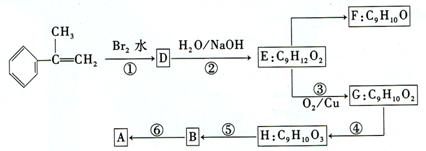
①写出反应类型:反应①属_______________反应,反应④属_______________反应,反应⑤属_______________反应。
②写出结构简式:D_______________,H_______________。
③已知在F分子中含“CH3OH”,通过F不能有效地、顺利地获得B,其原因是___________________________________________。
④写出反应方程式(注明必要的反应条件):
D→E:____________________________________________________________;
B→A:____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com