
科目: 来源: 题型:
已知某无色溶液只由Fe3+、Mg2+、Cu2+、Al3+、NH4+、Cl-、HCO3- 、OH-中的几种组成,向此溶液中加入一种淡黄色粉末状固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀。继续加入淡黄色粉末时,产生无刺激性气味的气体,白色沉淀只能部分溶解,则此溶液中一定大量含有的离子 ( )
A.Mg2+、Al3+、NH4+、Cl- B.Mg2+、Al3+、 NH4+
C.Mg2+、Cu2+、NH4+、HCO3- D.Mg2+、Cu2+、NH4+、Cl-
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列有关叙述正确的是 ( )
A.28g乙烯和28g丙烯分子中均含有6NA个共用电子对
B.在熔融状态下,1molNaHSO4完全电离出的阳离子数目为2NA
C.7.8gNa2O2中含有阴离子数目为0.2NA
D.在含4molC=O键的干冰晶体中,碳原子的数目为4NA
查看答案和解析>>
科目: 来源: 题型:
在一密闭容器中进行下列反应:2SO2+O2![]() 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达到平衡时,可能存在的数据是 ( )
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达到平衡时,可能存在的数据是 ( )
A.SO2为0.4mol/L,O2为0.2mol/L B.SO2为0.25mol/L
C.SO2,SO3均为0.15mol/L D.SO3为0.4mol/L
查看答案和解析>>
科目: 来源: 题型:
磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,制备时将含等物质的量的FeSO4和Fe2(SO4)3的溶液混合,再滴入稍过量的NaOH溶液,随后加入油酸钠溶液,即可生成黑色的、分散质粒子直径在55~36 nm的磁流体。下列说法中正确的是 ( )
A.所得的分散系属于悬浊液 B.该分散系能产生丁达尔效应
C.所得的分散系中分散质为Fe2O3 D.给分散系通直流电时,阳极周围黑色加深
查看答案和解析>>
科目: 来源: 题型:
无色的混合气体甲中可能含NO、CO2、NO2、NH3、N2中的几种.将100 mL气体甲经过下图实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为
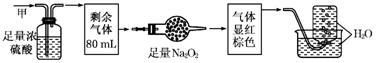
A.NH3、NO2、N2 B.NH3、NO、CO2 C.NH3、NO2、CO2 D.NO、CO2、N2
查看答案和解析>>
科目: 来源: 题型:
容积固定的密闭容器中,发生可逆反应:M(g)+N(g) ![]() 2P(g)+Q(g) ΔH>0,
2P(g)+Q(g) ΔH>0,
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1 mol·L-1,c(N)=2.4 mol·L-1,达到平衡后,M的转化率为60%,此时N 的浓度是 ,P 的体积分数为_________。
(2)若反应温度升高,M的转化率____________ (填“增大”“减小”或“不变”,下同),平均相对分子质量____________,混合气体密度____________。
查看答案和解析>>
科目: 来源: 题型:
2SO2(g)+O2(g) ![]() 2SO3(g)反应过程的能量变化如图所示。、
2SO3(g)反应过程的能量变化如图所示。、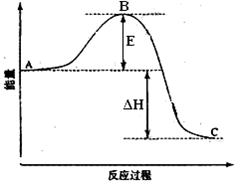
已知1mol SO2(g)氧化为1mol SO3的ΔH= -99kJ·mol—1.请回答下列问题:(1)图中A、C分别表示 、
,E的大小对该反应的反应热有无影响? 。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,并说明理由 ;
(2)图中△H= ;
(3)如果反应速率v(SO2)为0.05 mol·L—1·min—1,则v(O2)= mol·L—1·min—1
(4)已知单质硫的燃烧热为296 KJ·mol—1,计算由S(s)生成3 molSO3(g)的△H (要有计算过程)。
查看答案和解析>>
科目: 来源: 题型:
下列热化学方程式书写正确的是( )
A.C(s)+O2(g) = CO2(g);△H=+393.5 kJ·mol-1
B.2SO2+O2 = 2SO3;△H=-196.6 kJ·mol-1
C. 2H2(g)+O2(g) = 2H2O(l);△H=-571.6KJ
D.H2(g)+1/2O2(g) = H2O(l);△H=-285.8 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·x H2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2 。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2·x H2O的化学方程式为_________________________。
(2)检验TiO2·x H2O中Cl-是否被除净的方法是_________________________。
(3)下列可用于测定TiO2粒子大小的方法是____________(填字母代号)。
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
(4)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是______________;使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的_______(填字母代号)。

(5)滴定终点的现象是__________________________________________。
(6)滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为___________________。
(7)判断下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
① 若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果__ __。
② 若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com