
科目: 来源: 题型:
能用H++OH- = H2O表示的是 ( )
A.NaOH溶液和CO2的反应 B.Ba(OH)2溶液和稀H2SO4的反应
C.NaOH溶液和盐酸反应 D.氨水和稀H2SO4的反应
查看答案和解析>>
科目: 来源: 题型:
水的电离平衡曲线如图所示,下列说法不正确的是
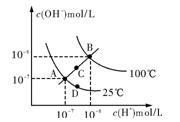
A.图中四点Kw间的关系:A=D<C<B
B.若从A点到C点,可采用:温度不变在水中加入少量NaAc固体
C.若从A点到D点,可采用:温度不变在水中加入少量酸
D.若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性
查看答案和解析>>
科目: 来源: 题型:
在某无色透明的酸性溶液中,能大量共存的离子组是( )
A.Na+ 、K+、SO42-、HCO3- B.Cu2+、K+、SO42--、NO3-
C.Na+、 K+、Cl-、 NO3- D.Fe3+、K+、SO42-、Cl-
查看答案和解析>>
科目: 来源: 题型:
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备
高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) ( )
A.阳极发生还原反应,其电极反应式:Ni2++2e-→Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
科目: 来源: 题型:
关于下列各装置图的叙述中,正确的是
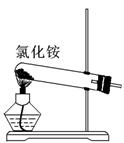


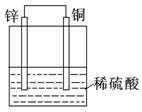
① ② ③ ④
A.实验室用装置①制取氨气
B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸
C.装置③可用于制备氢氧化亚铁并观察其颜色
D.装置④是原电池,锌电极为负极,发生还原反应
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列说法中不正确的是
A.20 gD2O中含有的中子数为10NA
B.3 g甲醛中含有的共价键数为0.4NA
C.14 g乙烯和丙烯的混合物中含有的原子总数为2NA
D.含NA个阳离子的CaC2固体投入足量水中,产生的乙炔为22.4L(标准状况)
查看答案和解析>>
科目: 来源: 题型:
有Ba Cl2和Na Cl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl―完全沉淀,反应中消耗x molH2SO4 ,y molAgNO3 。则原溶液中的钠离子浓度为( )
A.(y -2 x)/a B.(y–x)/a C.(2y -2 x)/a D.(2y -4x)/a
查看答案和解析>>
科目: 来源: 题型:
酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液与乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是:
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的衍生物
A.①③ B.②③ C.②④ D.①④
查看答案和解析>>
科目: 来源: 题型:
.已知常温下氯酸钾与浓盐酸反应放出氯气,KClO3 + 6 HCl = KCl + 3Cl2 ↑+3H2O。某校化学活动小组现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的颜色棉球,反应一段时间后,观察出:
(1).对图中指定部位颜色变化为
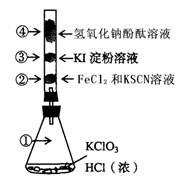
| ① | ② | ③ | ④ | |
| 颜色 |
(2).写出②中离子反应方程式_____________________________________.
写出④中离子反应方程式____________________________________________
(3).标出KClO3 + 6 HCl = KCl + 3Cl2 ↑+ 3 H2O反应中电子转移的方向和数目.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com