
科目: 来源: 题型:
下列实验操作正确且能达到预期目的的是
| 实验目的 | 操 作 | |
| 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 | |
| 欲证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 | |
| 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 | |
| 证明SO2具有漂白性 | 将SO2通入酸性KMnO4溶液中 | |
| 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu( NO3)2 的混合液 | |
| 确定碳和硅两元素非金属性强弱 | 测同温同浓度Na2CO3和Na2SiO3水溶液的PH |
A.①⑤⑥ B.①②⑥ C.①③④ D.②④⑥
查看答案和解析>>
科目: 来源: 题型:
常温时,0.1 mol·L-1的HA 溶液的pH=3 ,向该溶液中逐滴加入NaOH溶液,在滴加过程中,有关叙述不正确的是
A.未加入NaOH溶液时,原HA溶液中,c(H+) = c(OH-) + c(A-)
B.向原溶液中加水至溶液体积变为原体积的100倍时,所得溶液的pH大于3小于5
C.当滴入的NaOH与HA恰好完全中和时,溶液中c(Na+) = c(A-),且溶液呈中性
D.当加入过量的NaOH溶液时,溶液中离子浓度可能为:c(Na+)>c(A-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式正确的是
A.用![]() 溶液腐蚀印刷电路板:
溶液腐蚀印刷电路板:![]()
B.惰性电极电解氯化钠溶液:2Cl- +2 H2O ![]() Cl2 ↑+H2 ↑+2OH—
Cl2 ↑+H2 ↑+2OH—
C.氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.向Fe(OH)3悬浊液中加入醋酸:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目: 来源: 题型:
(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准)。
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
据表中数据,总结烯类化合物加溴时,反应速率与C=C上取代基的种类、个数间的关系:
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上类似,反应速率最慢的是________(填代号,1分)。
A、(CH3)2C=C(CH3) 2 B、CH3CH=CH CH3
C、CH2=CHCl D、CHF=CHCl
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3 + HBr ![]() CH3CHBrCH3 + CH3CH2CH2Br
CH3CHBrCH3 + CH3CH2CH2Br
(主要产物) (次要产物)
CH2=CH CH2CH3 + H2O → CH3CH(OH)CH2CH3 + CH3CH2CH2 CH2 OH
(主要产物) (次要产物)
化学式为C4H8的某烃A与HBr加成的主要产物中只含有一种氢原子。用结构简式表示A发生的反应方程式:
A 与水生成主要产物的反应
A的聚合反应
查看答案和解析>>
科目: 来源: 题型:
苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒。降脂等药效,主要酸性物质为苹果酸。苹果酸在分离提纯后的化学分析如下:①相对分子质量不超过150,完全燃烧后只生成CO2和H2O,分子中C、H质量分数分别为w(C)=35.82%。w(H)=4.48%;②1 mol该酸与足量的NaHCO3反应放出44.8 L CO2,与足量的Na反应放出33.6 L H2(气体体积均已折算为标准状况);③该分子中存在四种化学环境不同的碳原子,氢原子处于五种不同的化学环境。回答下列问题:
(1)苹果酸的分子式为 ,分子中有 个羧基。
(2)写出苹果酸的结构简式 。
(3)苹果酸的同分异构体中,符合上述①、②两个条件的有(写出结构简式): 、 。
查看答案和解析>>
科目: 来源: 题型:
化学和生活密切相关,下列叙述正确的是
A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
B.推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
C.氢能具有的优点是原料来源广、热值高、储存方便、制备工艺廉价易行
D.用聚苯乙烯全面代替木材,生产包装盒、快餐盒等以减少木材使用,保护森林
查看答案和解析>>
科目: 来源: 题型:
从下列事实所得出的结论或给出的解释正确的是( )
| 实验事实 | 结论或解释 | |
| ① | 将40 g NaOH溶于1 L蒸馏水中 | 该 溶液中溶质的质量分数为3.84%,其物质的量浓度为1molL-1 |
| ② | 向盛有1mL 0.1mol·L-1 AgNO3溶液的试管中滴加0.1molL-1 NaCl溶液,至不再有沉淀生成,再向其中滴0.1molL-1 KI溶液,白色沉淀转化为黄色沉淀。 | 常温下 Ksp(AgCl)< Ksp(AgI) |
| ⑶ | 某盐NaX溶液pH > 7 | 酸HX为弱酸 |
| ④ | 向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色 | 说明溶液中一定含有Fe2+ |
| ⑤ | 向盛有浓硝酸的试管中分别加入Al片和 Cu片,前者没有明显现象,后者反应剧烈,产生大量红棕色气体 | 还原性Al < Cu |
| ⑥ | BaSO4的水溶液导电性很差 | BaSO4是弱电解质 |
A.①④⑤ B.③④⑥ C.③④ D.②④⑥
查看答案和解析>>
科目: 来源: 题型:
pH=l的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积的关系如图,下列说法正确的是
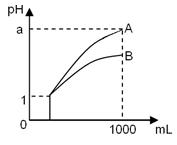
①若a<4,则A、B 都是弱酸
②稀释后,A酸溶液的酸性比B酸溶液强
③若a=4,则A是强酸,B是弱酸
④A、B两种酸溶液的物质的量浓度一定相等
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,正确的是
A. 化学反应中物质变化的实质是旧化学键的断裂和新化学键的形成
B. 离子化合物中一定有金属元素
C. 蛋白质溶液、淀粉溶液和葡萄糖溶液都是胶体
D. 共价化合物中各原子都一定满足最外层8电子稳定结构
查看答案和解析>>
科目: 来源: 题型:
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中该溶质的pC=-lg1×10-3=3。已知H2CO3溶液中存在的化学平衡为:CO2+H2O![]() H2CO3
H2CO3![]() H+ +HCO3—;HCO3—
H+ +HCO3—;HCO3—![]() H++CO32—。如图为H2CO3溶液的pC-pH图。请回答下列问题:
H++CO32—。如图为H2CO3溶液的pC-pH图。请回答下列问题:

(1)在pH=0~4时,H2CO3溶液中主要存在的离子为: ;在pH=12时,H2CO3溶液中主要存在的含碳阴离子为: ;
(2)pH<5时,溶液中H2CO3的pC值总是约等于3的原因是 ;
(3)一定浓度的NaHCO3和Na2CO3混合溶液是一种“缓冲溶液”,在这种溶液中加入少量的强酸或强碱,溶液的pH变化不大,其原因是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com