
科目: 来源: 题型:
始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式(线表示C—C键,端点、交点表示碳原子)如下图,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是( )
A.始祖鸟烯与乙烯互为同系物
B.若R1=R2=—CH3,则其化学式为C12H16
C.始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样的
D.若R1=R2,一定条件下烯烃双键碳原子上的氢也能取代,则始祖鸟烯环上的二氯代物有10种
查看答案和解析>>
科目: 来源: 题型:
已知:H2(g)+I2(g)![]() 2HI(g);△H < 0 有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
2HI(g);△H < 0 有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度 B.甲中加入0.1 mol He,乙不变
C.甲降低温度,乙不变 D.甲增加0.1 mol H2,乙增加0.1 mol I2
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.苯乙烯分子中所有原子可能在一个平面上
B.分子式为![]() 且分子中有苯环的有机物共有4种
且分子中有苯环的有机物共有4种
C.甲酸分子中有醛基,因此无法区别甲醛溶液和甲酸溶液
D.除去乙烯中混有的甲烷,可将混合气体通过酸性高锰酸钾溶液
查看答案和解析>>
科目: 来源: 题型:
对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成xmolNO的同时,消耗xmolNH3,则反应达到平衡状态
C.达到化学平衡时,若减小压强,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目: 来源: 题型:
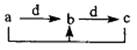
下表各组物中,物质之间通过一步反应就能实现如图所示转化的是 ( )
|
选项 | a | b | c | d |
| A | Al | Al(OH)3 | NaAlO2 | NaOH |
| B | CH3CH2OH | CH3CHO | CH3COOH | O2 |
| C | Na2CO3 | NaHCO3 | NaOH | CO2 |
| D | Cl2 | FeCl3 | FeCl2 | Fe |
查看答案和解析>>
科目: 来源: 题型:
可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4OH-
B.以NaOH溶液为电解液时,负极反应为:Al+3OH--3e-=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
科目: 来源: 题型:
已知污染性气体氮氧化物能用碱液除去,反应如下:
2NO2 + 2NaOH=NaNO2 +NaNO3+ H2O NO + NO2 + 2NaOH=2NaNO2 + H2O
根据硝酸尾气处理的反应原理,下列气体中不能被过量NaOH溶液完全吸收的是( )
A.1mol O2和4mol NO2 B.1mol O2和4mol NO
C.1mol NO和5mol NO2 D.4mol NO和1mol NO2
查看答案和解析>>
科目: 来源: 题型:
在T1℃时,向容积为2 L 的密闭容器甲中加人1mol N1、3mol H2及少量固体催 化剂,发生反应N2(g) + 3H2(g) ![]() 2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
(1) 该反应在0 ~l0min 时间内H2的平均反应速率为______,N2的转化率为______。
 (2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
(2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
a.大于25% b.等于25% c.小于25%
(3)右图是在T1℃时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在T2℃(T1 >T2)时H2的体积分数随时间t的变化曲线。
(4)若保持T1℃,在体积也为2 L 的密闭容器乙中通入一定量的N2、H2、NH3,欲使平衡时容器乙中各物质的物质的量与容器甲中完全相同,且起始时反应向正反应方向进行,则通入H2的物质的量x的取值范围是____________。
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.4.0g碳化硅晶体中所含C—Si数为0.4NA
B.PCl3、BF3、HClO这些分子中每个原子都达到了8电子结构
C.电解精炼铜时,当阳极质量减少3.2 g时,电路中转移的电子数为0.1NA
D.若H+(aq) + OH-(aq)= H2O(l);![]() kJ·mol-1,则含Ba(OH)2 1 mol溶液与1 mol稀H2SO4反应放出的热量为114.6 kJ
kJ·mol-1,则含Ba(OH)2 1 mol溶液与1 mol稀H2SO4反应放出的热量为114.6 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com