
科目: 来源: 题型:
某燃料电池所用燃料为H2和空气,电解质为熔融的K2CO3。该电池的总反应为2H2+O2 2H2O,负极反应为H2+CO32――2e- H2O+CO2。下列说法正确的是( )
A.放电时CO32-向负极移动
B.该电池正极反应式为:4OH――4e- 2H2O+O2↑
C.电池放电时,电池中CO32-数目逐渐减少
D.电池放电时,电子经正极、负极、熔融的K2CO3后再回到正极,形成闭合回路
查看答案和解析>>
科目: 来源: 题型:
(附加题)(共10分)(1)室温下取0.2mol·L-1HCl溶液与0.2mol·L-1 MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
① 混合溶液中水电离出的c(H+)__________0.2mol·L-1 HCl溶液中电离出的c(H+);(填“>”、“<”、或“=”)
② 求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-) - c(M+) = ______________ mol·L-1
c(H+) - c(MOH) = _______________ mol·L-1
(2)室温下如果取0.2mol·L-1 MOH溶液与0.1 mol·L-1 HCl溶液等体积混合,测得混合溶液的pH<7,则说明MOH的电离程度________MCl的水解程度。(填“>”、“<”、或“=”),溶液中各离子浓度由大到小的顺序为______________
查看答案和解析>>
科目: 来源: 题型:
下列关于工业合成氨3H2+N2(g)![]() 2NH3(g)(正反应为放热反应)叙述中不正确的是
2NH3(g)(正反应为放热反应)叙述中不正确的是
A.选择适宜温度,可以提高催化剂的活性
B.氮气和氢气的循环使用,可以提高原料的利用率
C.高压比常压更利于合成氨的反应
D.降低平衡混合气温度,可以使反应速率增大,氨的产量提高
查看答案和解析>>
科目: 来源: 题型:
下列关于反应限度的叙述不正确的是( )
A.反应限度是一种平衡状态,此时反应已经停止
B.达到平衡状态时,正反应速率和逆反应速率相等
C.达到平衡状态时,反应物和生成物浓度都不再改变
D.不少反应都具有可逆性,只是有的程度小,有的程度大
查看答案和解析>>
科目: 来源: 题型:
高温下用碳还原某金属氧化物MO2,在标准状况下,得到400mLCO、100mLCO2和0.978g金属M,则M的相对原子质量为 ( )
A.40 B.73 C.118 D.207
查看答案和解析>>
科目: 来源: 题型:
开瑞坦是治疗过敏性鼻炎的良药,其有效成分的结构简式如图所示。下列有关说法正确的是 ( )
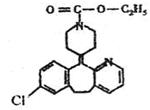
A.该有机物易溶于水
B.分子中含有四个六元环,其中有一个是苯环
C.1mol分子水解后只能得到2mol产物
D.1mol分子最多能与7molH2发生加成反应
查看答案和解析>>
科目: 来源: 题型:
在一密闭容器中有CH4和O2混合气体共20g,放入足量Na2O2用电火花引燃,使其完全反应,Na2O2增重8g,则原混合气体中O2的质量分数是( )
A.33.3% B.40% C.60% D.80%
查看答案和解析>>
科目: 来源: 题型:
无水CuSO4在强热下会发生分解反应:
CuSO4![]() CuO + SO3↑
CuO + SO3↑
2SO3![]() 2SO2↑+ O2↑
2SO2↑+ O2↑
某研究性学习小组设计了下图所示装置(夹持仪器已略去),利用D管在反应前后的质量差计算分解的无水CuSO4的质量。

实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一定时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的空气。
④再称量D管,得其反应前后的质量差为m。
(1)B管中出现的现象是__________________________________________________。
有关离子方程式是__________________________________________________
(2)B管的作用是除去混合气体中的SO3,实验过程中发现B管的温度明显升高,主要原因是______________________
(3)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算分解的无水CuSO4的质量?___________
原因是__________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应式为:2H2+O2=====2H2O,下列有关说法正确的是 ( )

A.电子通过外电路从b极流向a极
B.b极上的电极反应式为:O2+2H2O+4e-====4OH-
C.每转移0.1mol电子,消耗1.12L的H2
D.H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com