
科目: 来源: 题型:
在有机物分子中,若某个碳原子连接4个不同的原子或原子团,则这种碳原子称为“手性碳原子”。凡有一个手性碳原子的物质一定具有光学活性。物质: ![]() 有光学活性,它发生下列反应后生成的有机物仍有光学活性的是
有光学活性,它发生下列反应后生成的有机物仍有光学活性的是
A.与NaOH溶液共热 B.与甲酸发生酯化反应
C.铜作催化剂的条件下被氧气氧化 D.在催化剂存在下与H2作用
查看答案和解析>>
科目: 来源: 题型:
某可逆反应进行过程中,在不同反应时间各物质的量的变化情况如图所示。则该反应的化学方程式为 ;反应开始至2分钟,能否用C表示反应速率吗? (填“能”或不能”),原因 。

查看答案和解析>>
科目: 来源: 题型:
在一恒定的容器中充入2molA和1molB发生反应:2A(g)+B(g) ![]() xC(g),达平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为W%,则x值为
xC(g),达平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为W%,则x值为
A.只能为2 B.只有为3 C.无法确定 D.可能是2,也可能是3.
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E为短周期元素组成的中学常见物质,它们转化关系如图所示(部分产物、条件略去)。
下列说法正确的是( )
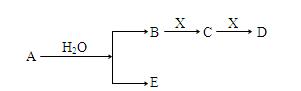
A.若C为二氧化碳,则E可以是强碱也可以是强酸
B.若D为白色胶状难溶物,且与A摩尔质量相等,则E为一常见气体单质
C.若E为氢气,则A一定为金属单质钠
D.若A为金属单质,则X一定为二氧化碳
查看答案和解析>>
科目: 来源: 题型:
某同学进行了如图所示的实验,由实验现象得到的结论中正确的是

A. 原溶液中一定只含有SO![]()
B. 原溶液中一定含有SO![]() 和Cl—
和Cl—
C. 原溶液中一定只含有Cl—
D. 原溶液中可能含有SO![]() ,也可能含有Cl—
,也可能含有Cl—
查看答案和解析>>
科目: 来源: 题型:
标准状况下分别向甲、乙、丙三个容器中加入30.0 mL同浓度的盐酸,再加入不同质量的由两种金属组成的同种合金粉末,测量放出气体的体积。另在甲、乙、丙三个容器中加入30.0 mL与盐酸同浓度的氢氧化钠溶液,再分别加入与上述实验相同质量的同种合金,测量放出气体的体积。所得数据如下表所示:
| 反应容器 | 甲 | 乙 | 丙 |
| 合金的质量/g | 0.510 | 1.53 | 3.57 |
| 与盐酸反应产生气体的体积/L | 0.560 | 0.672 | 0.672 |
| 与氢氧化钠反应产生气体的体积/L | 0.336 | x | y |
根据表中数据不可能得出的结论是
A.盐酸的物质的量浓度为2 mol·L-1 B.合金可能由镁与铝组成
C.x=2.016 D.y=2.016
查看答案和解析>>
科目: 来源: 题型:
某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC—COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸)为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华。为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1 mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生。该反应的离子方程式为_______________________________________。
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有_____________(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式:____ MnO4– + ____ H2C2O4 + _____ H+ = _____ Mn2+ + _____ CO2↑ + _____ H2O
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):

实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:
上述装置中,D的作用是__________________。
乙二酸分解的化学方程式为____________________________________________。
(4)该小组同学将2.52 g草酸晶体(H2C2O4·2H2O)加入到100 mL 0.2 mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是______________________________。(用文字简单表述)
(5)以上溶液中各离子的浓度由大到小的顺序为: _____________________;(用离子符号表示)
查看答案和解析>>
科目: 来源: 题型:
以下是对某水溶液进行离子检验的方法和结论,其中正确的是
A.先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀。溶液中一定含有大量的SO42-
B.加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定有大量的CO32-
C.用洁净的铂丝蘸取该溶液,置于火焰上灼烧,透过蓝色钴玻璃能观察到火焰呈紫色。该溶液中一定含有钾离子,可能含有钠离子。
D.先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl-
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F六种短周期元素,原子序数依次增大。A、E同主族,元素原子的核外电子数是A元素原子核内质子数的两倍。B、C两元素原子的最外层电子数之和等于D元素原子的最外层电子数,C、D两元素原子最外层电子数之和等于F元素原子的最外层电子数。D元素原子最外层电子数是次外层电子数的一半。
回答下列问题:
⑴ 用电子式表示B、F两元素形成化合物的过程: ;
⑵ A、C两元素的化合物与B的氢氧化物反应的离子方程式为 ;
⑶ D气态氢化物的稳定性 (填“大于”、“小于”)E的气态氢化物的稳定性。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com