
科目: 来源: 题型:
下列叙述中正确的是
A.体积相同、浓度均为0.1mol/L的NaOH溶液、氨水,分别稀释m倍、n倍,溶液的pH都变成9,则m<n
B.有甲、乙两醋酸溶液,测得甲的pH=a,乙的pH=a+1,若用于中和等物质的量浓度等体积的NaOH溶液,需甲、乙两酸的体积V(乙)>10V(甲)
C.25℃,pH=9的NaOH溶液和NaAc溶液中,由水电离出的c(H+)均为10-5mol·L-1
D.c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)该式满足NaHCO3溶液中的离子浓度关系。
查看答案和解析>>
科目: 来源: 题型:
1下列哪一项符合“绿色化学”的原则
A.排放前对废气、废水、废渣进行无害化处理
B.在化学生产中少用或不用有害物质以及少排放或不排放有害物质
C.在化工生产中,尽量避免使用任何化学物质
D.在化工厂范围多种草种树,努力构建花园式工厂
查看答案和解析>>
科目: 来源: 题型:
合成氨反应为:N2(g)+3H2(g) ![]() 2NH3(g)。图1表示在一定的温度下此反应过程中
2NH3(g)。图1表示在一定的温度下此反应过程中
的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。
图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
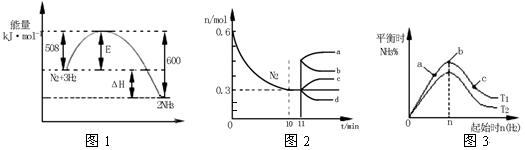
下列说法正确的是:
A.该反应为自发反应,由图1可得加入适当的催化剂,E和△H都减小
B.图2中0~10min内该反应的平均速率v(H2)=0.045mol·L-1·min-1,从11min起其
它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为d
C.图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点
D.图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2
查看答案和解析>>
科目: 来源: 题型:
在盛有水的电解槽中加入等物质的量的AgNO3、Ba(NO3)2、Na2SO4、MgCl2,摇匀后用惰性电极电解,最初得到的氧化产物与还原产物的质量比为( )
A.71:2 B.71:216 C.8:1 D.16:137
查看答案和解析>>
科目: 来源: 题型:
下列化学方程式中,能用离子方程式:H+ + OH- = H2O表示的是
Mg(OH)2 + 2 HCl = Mg Cl2 + 2 H2O
B.2 NaOH + H2SO4 = Na2SO4 + 2 H2O
C.Ba(OH)2 + H2SO4 = BaSO4 ↓ + 2 H2O
D.2 HCl + Cu(OH)2 = CuCl2 + 2 H2O
查看答案和解析>>
科目: 来源: 题型:
右图是一种染料敏化太阳能电池的示意图,电池的一个电极由有机光敏染料(S)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为: 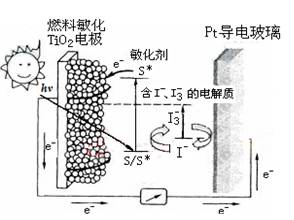
TiO2/S→TiO2/S*(激发态)
TiO2/S*→TiO2/S++e-
I3-+2e-→3I-
2TiO2/S++3I-→2TiO2/S+I3-
下列关于该电池叙述错误的是:
A、电池工作时,I-离子在镀铂导电玻璃电极上放电
B、电池工作时,是将太阳能转化为电能
C、电池的电解质溶液中I-和I3-的浓度不会减少
D、电池中镀铂导电玻璃为正极
查看答案和解析>>
科目: 来源: 题型:
(1)49 g硫酸的物质的量为 mol,若在水中完全电离可产生 molH+ , ______mol![]() .若有一定量的硫酸完全电离产生
.若有一定量的硫酸完全电离产生![]() 个
个![]() ,此硫酸的质量为 _______g.
,此硫酸的质量为 _______g.
(2)标准状况下,11.2L的H2S气体质量为17g,则H2S的摩尔质量是 ,相对分子质量为 ; 等物质的量的NH3与H2S质量比为 ; 1.7g氨气与 mol H2O含有的电子数相等。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com