
科目: 来源: 题型:
下列各组中化合物的性质比较,不正确的是( )
A.酸性:HClO4>HBrO4>HIO4 B.碱性:NaOH>Mg(OH)2>Al(OH)3
C.稳定性:PH3>H2S> HCl D.非金属性:F>O>S
查看答案和解析>>
科目: 来源: 题型:
某有机物A可发生下列变化。已知C为羧酸,且C、E不发生银镜反应,则A的
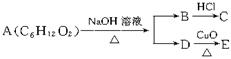
可能结构为
A.![]() B.
B.![]()
C.CH3CH2COOCH2CH2CH3 D.HCOO(CH2)4CH3
查看答案和解析>>
科目: 来源: 题型:
如下图所示,用排饱和食盐水法先后收集20ml CH4 和80ml Cl2,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,观察发生的现象。回答下列问题:

(1)大约30min后,可以观察到量筒壁上出现 状液体,该现象说明生成了 (填序号)
①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4
量筒内出现的白雾是 ,量筒内液面 (填“上升”、“下降”或“不变”)
(2)使0.5摩尔甲烷和氯气发生取代反应,生成相同物质的量的四种有机取代物,则需要氯气的物质的量是
A.2.5mol B.2 mol C.1.25 mol D.0.5 mol
(3)液化石油气的主要成分是丙烷,试写出丙烷燃烧的化学方程式 。
将现用液化石油气的燃具改用天然气时应 进空气的风口。(填增大或减少)
(4)下列烷烃的分子式有 3种同分异构体的是 。(填字母)
A.C5H12 B.C4H10 C.C3H8 D.C2H6
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是 ( )
A.在配制硫化钠溶液时,为了防止发生水解,可以加入少量的KOH
B.用润湿的精密pH试纸测硫酸铝溶液的pH,测定结果偏小
C.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸
D.中性溶液中水的电离程度不一定比酸性溶液中水的电离程度大
查看答案和解析>>
科目: 来源: 题型:
验证淀粉水解可生成葡萄糖,进行了下列实验,该实验中操作步骤的排列顺序正确的是①取少量淀粉加水制成溶液 ②加热煮沸 ③加入Cu(OH)2悬浊液 ④加入几滴稀硫酸 ⑤再加热 ⑥加入NaOH溶液,调PH至碱性 ( )
A.④②⑥③⑤ B.①⑤②⑥④③
C.①②④⑤③⑥ D.①④②⑥③⑤
查看答案和解析>>
科目: 来源: 题型:
水的电离平衡曲线如下图所示。?
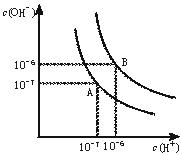
(1)若以A点表示25℃时水在电离平衡时的离子浓度, 当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将常温下的pH=8的Ba(OH)2溶液与常温下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为 。
(3)已知AnBm的离子积=[c(Am+)]n·[c(Bn-)]m?,式中c(Am+)n和c(Bn-)m表示离子的物质的量浓度。在某温度下,Ca(OH)2的溶解度为0.74 g,其饱和溶液密度设为1 g/mL,其离子积为 。
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组查阅资料得知:漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(C1O)2+CaCl2+H2SO4![]() 2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
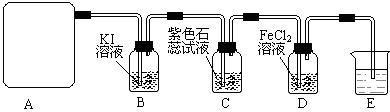
试回答下列问题:
(1)每生成1 mol Cl2,上述化学反应中转移的电子个数为______ (NA表示阿伏加德罗常数)。
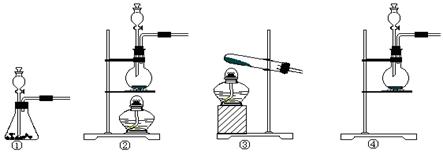
(2)该实验中A处可选用装置__________ _____ (填写装置的序号)。
(3)装置B中发生反应的离子方程式为________________________________________。
(4)装置C中的现象为___________________________________________________,
试结合反应方程式解释其原因 __________________________________ _
_________________________________ 。
(5)装置E中的试剂是______________(任填一种合适试剂的名称),其作用是________
_______________________________ ______。
(6)请帮助该学习小组同学设计一个实验,证明装置D中有FeCl3生成(请简述实验步骤)
_________________________________________________________________________
___________________________________________________ ______________
查看答案和解析>>
科目: 来源: 题型:
某含氧有机物,它的相对分子质量为74。7.4g该含氧有机物充分燃烧后的产物通过浓硫酸后增重5.4g,通过足量澄清石灰水后有30g白色沉淀生成。求:
(1)该含氧有机物的分子式;
(2)该含氧有机物有多种同分异构体,写出其中能水解的同分异构体的结构简式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com