
科目: 来源: 题型:
向下列溶液滴加稀硫酸,生成白色沉淀,继续滴加氢氧化钠溶液,沉淀又溶解的是( )
A. Na2SiO3 B. BaCl2 C. FeCl3 D. NaAlO2
查看答案和解析>>
科目: 来源: 题型:
下列事实不能用勒沙特列原理解释的是
A.合成氨工业选择的反应条件不是室温,是500℃左右
B.配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释
C.实验室常用排饱和食盐水的方法收集氯气
D.硫酸工业中,使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目: 来源: 题型:
下列有水参加的反应中,属于加成反应的是 ( )
A.C12H22O11(蔗糖)+H2O![]() C6H12O6(葡萄糖)+C6H12O6(果糖)
C6H12O6(葡萄糖)+C6H12O6(果糖)
B.CH3CH2ONa+H2O![]() CH3CH2OH+NaOH
CH3CH2OH+NaOH
C.CH2=CH2+H2O ![]() CH3CH2OH
CH3CH2OH
D.CaC2+2H2O![]() Ca(OH)2+C2H2↑
Ca(OH)2+C2H2↑
查看答案和解析>>
科目: 来源: 题型:
下列有关说法中正确的是 ( )
A.因为酒精能消耗,所以喝白酒可以防止甲流H1N1
B.因为苯酚具有杀菌能力,所以自来水可以用苯酚消毒处理
C.因为SiO2是酸性氧化物,所以其不和任何酸发生反应
D.因为明矾在水中能水解形成Al(OH)2胶体,所以明矾可用作净水剂
查看答案和解析>>
科目: 来源: 题型:阅读理解
硫化钠和碳酸钠为原料、采用下述装置制备硫代硫酸钠,制备反应可表示为:
2Na2 S +Na2CO3 + 4SO2 ![]() 3Na2S2O3 +CO2。根据要求回答问题:
3Na2S2O3 +CO2。根据要求回答问题:
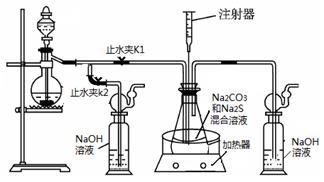
(1)实验时,打开K1,关闭K2,最后洗气瓶中发生反应的离子方程式是 。
(2)锥形瓶内溶液pH小于7时会导致产品分解,因此实验过程中需要控制锥形瓶内溶液的pH。
①反应过程中,锥形瓶中溶液pH将________(填“增大”、“减小”或“保持不变”)。
②测量锥形瓶中溶液pH时,用注射器吸取溶液样品比直接打开锥形瓶中瓶塞取样,除操作简便外,还具有的优点是 。
③若实验过程中测得溶液pH已接近于7。此时应该进行的操作是 。
(3)已知:2Na2 S2O3 +I2=2NaI+ Na2 S4O6。实验结束后进行相关处理,可即获得Na2 S2O3 ·5H2O晶体。为测量其纯度,取晶体样品mg,加水溶解后,滴入几滴淀粉溶液,用0.010mol/L碘水滴定到终点时,消耗碘水溶液vmL,则该样品纯度是 。
(4)制取硫代硫酸钠的另一种方法是直接将硫粉和亚硫酸钠、水混合共热制取。为探究制取硫代硫酸钠最佳条件(溶液pH、亚硫酸钠浓度、反应温度、硫粉质量),设计如下对比实验(每次实验时亚硫酸钠质量均为63g,反应时间为30min):
| 实验序号 | 溶液pH | 亚硫酸钠与水的质量比 | 反应温度 | 硫粉质量 | 亚硫酸钠转化率 |
| 1 | 10 | 1.5:1 | 100 | 18 | 80.7% |
| 2 | a | 1.1:1 | 100 | 18 | 94.6% |
查看答案和解析>>
科目: 来源: 题型:
. 已知A、E、I、L是常见的非金属单质,其中A为淡黄色固体;Z是常见的金属单质,B的相对分子质量比A大32,C的相对分子质量比B大16,Y是一种常见的液体,J是磁性氧化铁, D、H、K均是重要的化工产品;X分子的球棍模型如下左图,组成X的两种元素的相对原子质量相差18。下列框图中部分反应条件已略去。
试回答下列问题:
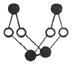
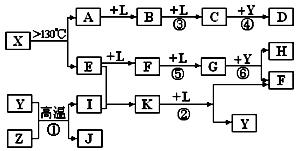
(1)下列有关X的说法正确的是 .
A.该物质的分子式为S4N4
B.该物质的分子中既有极性键又有非极性键
C.该物质具有很高的熔、沸点
D.该物质与化合物S2N2互为同素异形体
(2)E的电子式为 ,D的分子式 ,在反应①、②、③、④、⑤、⑥中属于非氧化还原反应的是 。(填序号)
(3)写出反应②的化学方程式: 。
(4)J与过量H的稀溶液反应的离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
在给定条件下,下列加线的物质在化学反应中能被“全消耗”的是( )
A.用50mL 12mol/L盐酸与过量的二氧化锰共热制取氯气
B.向100mL 3mol/L的硝酸中加入5. 6g铁粉
C.标准状况下,将1g铝片投入20mL 18. 4mol/L的硫酸中
D.在5 ×107 Pa、500℃和铁触媒催化的条件下,用2mol氮气和3mol氢气合成氨
查看答案和解析>>
科目: 来源: 题型:
在0.1 mol·L-1Na2CO3溶液中,下列关系正确的是 ( )
A.c(Na+)>c(CO32一)>c(OH一)>c(HCO3一)>c(H+)
B.c(Na+)+c(H+)=c(HCO3一)+c(CO32-)+c(OH一)
C.c(Na+)>c(CO32一)>c(HCO3-)>c(H+)>c(OH一)
D.c(HCO3一)+2c(CO32一)+c(H2CO3)=0.1 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com