
科目: 来源: 题型:
在标准状况下,三个干燥的烧瓶内分别装入:干燥纯净的NH3、含有部分空气的HCl气体、体积比为4:10的NO2与O2的混合气体。分别做喷泉实验,最终三个烧瓶中所得溶液的物质的量浓度(假设溶液不外渗)之比为( )
A.2:1:2 B.5:5:4 C.1:1:1 D.无法确定
查看答案和解析>>
科目: 来源: 题型:
下列化学用语正确的是
A、表示乙炔“燃烧热”对应的热化学方程式:
C2H2(g)+![]() O2(g) = 2CO2(g)+H2O(g);??△H =-1 256 KJ/mol
O2(g) = 2CO2(g)+H2O(g);??△H =-1 256 KJ/mol
B、Na2O2的电子式:![]()
C.卤化氢都极易溶于水,溶液均为强酸
D、表示中和热的热化学方程式:NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l) ; △H = -57.3kJ/mol
Na2SO4(aq)+H2O(l) ; △H = -57.3kJ/mol
查看答案和解析>>
科目: 来源: 题型:
某无色溶液,其中可能存在如下离子:Na+.Ag+.Ba2+.Al3+.AlO2―.S2―.CO32―.SO32―.SO42―,现取该溶液进行有关实验,结果与下图所示。
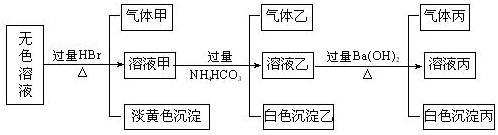
试回答下列问题:
(1)生成沉淀甲的离子方程式为 。
(2)由溶液甲生成沉淀乙的离子方程式 。
(3)沉淀丙是 。如何用一化学实验来确定其成分
(4)气体甲的成分有哪几种可能 。
(5)综合上述信息,可以肯定存在的离子有 ,一定不存在的离子是 ,可能存在的离子是 。
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式正确的是
A.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.用石墨作电极电解饱和食盐水: 2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O
D.FeSO4溶液中加H2O2溶液: Fe2++2H2O2+4H+=Fe3++4H2O
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组用含铝、铁、铜的合金废料制取纯净的氯化铝溶液、绿矾晶体(FeSO4??7H2O)和胆矾晶体(CuSO4??5H2O),方案如下:
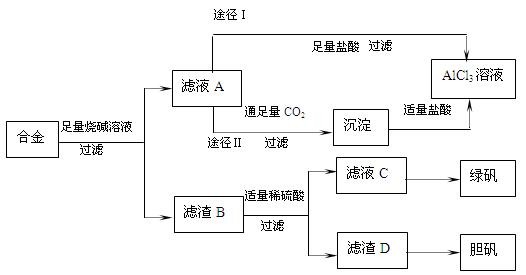
(1)写出合金溶于足量烧碱溶液时相关反应的离子方程式 ;
(2)从滤液C中得到绿矾的实验操作是蒸发浓缩、 、过滤、洗涤等。
(3)H2O2是一种应用广泛的绿色氧化剂,往滤渣D中加入稀硫酸和H2O2可以制备胆矾晶体,该反应的总化学方程式为 。
(4)由滤液A通过途径I和途径II都可得到AlCl3溶液,从产品纯度角度考虑,你认为最合理的是 (填“途径I”或“途径II”),理由是 。
(5)若上述方案所用的稀硫酸溶质质量分数为36.8%,那么100mL98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸 g。
查看答案和解析>>
科目: 来源: 题型:
有下列两种转化途径,某些反应条件和产物已省略,下列有关说法不正确的是

A.途径①反应中体现了浓HNO3的强氧化性和酸性
B.途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本
C.由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e-
D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高
查看答案和解析>>
科目: 来源: 题型:
C、D、G、I均为短周期元素形成的单质,D、G、I为常见非金属气态单质。D元素的原子的最外层电子数是次外层电子数的3倍,C、G同周期,且原子最外层电子数相差4,它们的简单离子电子层结构不同。相互间有如下转化关系:

请填空:
(1) D与I能形成原子个数比为1:1的共价化合物,请写出其分子式: ;
(2)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,写出电解E水溶液的化学式: 。
(3)化合物K 中含有组成单质L的元素,且该元素的质量分数为70%。反应①的化学方程式是 ,引发该反应的操作是
(4)写出A+F → J的离子方程式: 。
查看答案和解析>>
科目: 来源: 题型:
在A.B两个大小相同,温度相同的密闭容器中,充入x mol和y mol的SO3(g)(x>y),分别发生分解反应:2SO3(g) ![]() 2SO2(g)+O2(g),达到平衡时,其分解率分别为a%和b%,a b关系正确的是( )
2SO2(g)+O2(g),达到平衡时,其分解率分别为a%和b%,a b关系正确的是( )
A.a=b B.a<b C. a>b D.无法比较
查看答案和解析>>
科目: 来源: 题型:
钠和铝是两种重要的金属。请回答:
(1)将一小块金属钠投入水中,可观察到的实验现象是_____________(填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(2)铝与氢氧化钠溶液反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com