
科目: 来源: 题型:
将100gK2CO3和KHCO3的混合物加热至质量不再变化时,共收集到CO211g,原混合物中KHCO3的质量分数是( )
A.30% B.40% C.50% D.60%
查看答案和解析>>
科目: 来源: 题型:
a是盛有标准状况下的空气(氧气占1/5)和10mL 1.2mol/L硝酸的250 mL烧瓶;b是未充气(实验开始前内部没有气体)放有0.384g铜粉的气球;c是夹紧了的弹簧夹;d中盛有足量的过氧化钠;e是充有二氧化碳的针筒。整套装置已经过气密性检查合格。
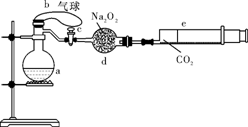
(1)将气球中的铜粉小心倒入烧瓶中,充分反应后发现铜粉有余(设产生的气体不溶解于溶液中),则可观察到的现象是 。
(2)欲提高铜与硝酸反应的速率可采用多种不同的措施。
①若用加入化学试剂法,下列试剂中可以选用的是 。
A.蒸馏水 B.无水醋酸钠
C.石墨 D.少量硝酸银溶液
②将烧瓶不断振荡发现气球逐渐缩小,反应的化学方程式是4NO2+O2+2H2O===4HNO3 或4NO+3O2+2H2O===4HNO3 ,此时气球是全在烧瓶外还是一部分进入烧瓶 。
③打开弹簧夹,将二氧化碳反推入干燥管内继续振荡,使气体与气体、溶液充分接触,欲使所有的铜粉全溶解,至少需要推入二氧化碳 mL。
④将上述全过程用一个总的化学方程式表示: 。
查看答案和解析>>
科目: 来源: 题型:
下列大小顺序排列完全正确的组合是( )
①气态氢化物的稳定性:HF>NH3>PH3
②沸点:CH4>C3H8>CH3OH
③离子半径:K+>Ca2+>S2-
④相同温度、相同浓度溶液中水的电离程度:NH4Cl>CH3COOH>HCl
A.①② B.①④ C.②③ D.③④
查看答案和解析>>
科目: 来源: 题型:
著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献。已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快反应。(注:铈常见的化合价为+3和+4,氧化性:Ce 4+>Fe 3+>I2。)下列说法正确的是( )
A.铈溶于氢碘酸的化学方程式可表示为:Ce + 4HI=CeI4 + 2H2↑
B.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4+ + 2Fe2+ = Ce3+ + 2Fe3+
C.在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得铈
D.四种的核素136 58Ce、138 58Ce、140 58Ce、142 58Ce,它们互称为同素异形体
查看答案和解析>>
科目: 来源: 题型:
下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是: ( )
| 物质 编号 | 甲 | 乙 | 丙 | 丁 | 物质转化关系 |
| A | Cu | CuCl2 | CuO | Cu(NO3)2 |
|
| B网] | Na2CO3[来 | NaOH | NaHCO3[] | CO2 | |
| C | Fe | Fe Cl3 | Fe(OH)3 | Fe2O3 | |
| D | Al2O3 | Al(OH)3 | NaAlO2 | AlCl3 |
查看答案和解析>>
科目: 来源: 题型:
已知1mol白磷变成1mol红磷时放出热量18.39kJ,则下列两个反应中:
4P(白,s)+5O2(g)=2P2O5(s) △H=-Q1kJ/mol
4P(红,s)+5O2(g)=2P2O5(s) △H=-Q2kJ/mol
Q1和Q2的关系正确的是
A.Q1= Q2 B.Q1>Q2 C.Q1<Q2 D.无法确定
查看答案和解析>>
科目: 来源: 题型:
钢铁工业是国家工业的基础,请回答:钢铁冶炼、腐蚀与防护过程中的有关问题。
(1)工业用热还原法冶炼生铁的主要原料有 ,设备的名称是 写出用还原剂CO还原赤铁矿(主要成分为Fe2O3)的化学方程式
。
(2)写出钢铁在潮湿空气中发生锈蚀时的正极反应方程式
生成铁锈(Fe2O3..XH2O)的化学方程式为 .
(3)生铁的用途远远不及钢材广泛,人们把较多的高炉生铁直接冶炼成钢,由生铁直接在纯氧顶吹转炉中转化成钢时,是把有害杂质除掉而保留有益元素,可以概括为
。为了防止钢铁制品发生锈蚀,可以在钢铁零件的表面进行电镀铜等措施,电镀铜时的阳极反应为 。
查看答案和解析>>
科目: 来源: 题型:
下列各组离子能在指定溶液中大量共存的是 ( )
①酸性溶液中:Fe2+,Al3+,NO3-,I-,S2-
②在pH=11的溶液中:Na+,AlO2-,NO3-,S2-,SO32-
③由水电离的c(H+)=1×10-13mol/L的溶液中:Cl-,HCO3-,NO3-,NH4+,S2O32--
④加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42-
⑤使甲基橙变红的溶液中:Fe3+,MnO4-,NO3-,Na+,SO42-
⑥无色溶液中:K+,Cl-,Na+,H2PO4-,PO43-
A.①②⑤ B.①③⑥ C.②④⑤ D.①②④
查看答案和解析>>
科目: 来源: 题型:
下列反应所产生的气体体积在标准状况下为22.4L的是 ( )
A.将2mol金属Cu与含2molH2SO4的浓硫酸共热
B.将1 mol MnO2固体与含4molHCl的浓盐酸共热
C.常温下,将32.2g金属钠和5.4g金属铝同时投入到足量水中
D.常温下,将10.8g的Al和22.4g的Fe投入到300g 98%的硫酸中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com