
科目: 来源: 题型:
实验室需要制备纯净的氯化钾。现有含少量KBr和K2SO4的氯化钾样品,按照下图所示的实验方案进行提纯。

请回答下列问题:
(1)操作I的名称为 ,操作II所需要的玻璃仪器有 。
(2)若用硝酸钡来代替氯化钡,是否可行?请说明理由。
。
(3)若实验所得固体甲、乙的质量分别为W 1g和W 2g,则样品中KBr的质量分数计算式为 。
(4)某同学对该实验方案提出质疑,他认为加适量氯化钡溶液不容易控制,应该加入过量氯化钡溶液,请你按照他的思路,用上述实验流程图表示出他后面的实验过程,要注明所用试剂和所得产物的化学式以及相应操作的名称。

查看答案和解析>>
科目: 来源: 题型:
下列各组离子,在所给条件下一定能够大量共存的是____________
(1)pH=7的溶液中:Fe3+、Mg2+、NO3-、SO42-
⑵ 加入苯酚显紫色的溶液中:Na+、Mg2+、Cl-、SO42-
(3)能和Ca2+生成沉淀的溶液中:K+、Ba2+、CH3COO-、Cl-
(4)加入铝粉能放出氢气的溶液中:CO32-、AlO2-、I-、NO3-
(5)c(H+)/ c(OH-)=1012的溶液中:NH4+ 、Al3+、Ca2+、Cl-
(6)常温下,c(H+)/c(OH-) = 10-10的溶液中:Ca2+、Mg2+、ClO-、I-
(7)在含有大量HCO3―的溶液中:K+、Na+、AlO2- 、Br-
(8) 在使pH试纸变红的溶液中:Fe2+、Na+、SO42 -、NO3-
查看答案和解析>>
科目: 来源: 题型:
锂被誉为“高能金属”。工业上用硫酸与β-锂辉矿(LiAlSi2O6和少量钙镁杂质)在250~300℃反应,生成Li2SO4以及硅铝化合物、MgSO4等,其工业生产流程如下:
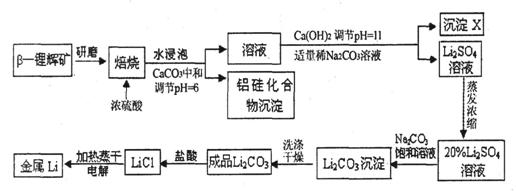
(1)用氧化物形式表示LiAlSi2O6的组成:___________________。
(2)沉淀X的主要成分是(写化学式)________________________。
(3)流程中两次使用了Na2CO3溶液,试说明前后浓度不同的原因:________________。
(4)锂和氢气在加热时能反应生成白色固体氢化锂,氢化锂遇到水就立即溶解并释放出大量的气体。试写出氢化锂遇水反应的化学方程式:______________________。
(5)将盐酸与Li2C03完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂。电解时产生的氯气中会混有少量氧气,原因是_____________________________。
查看答案和解析>>
科目: 来源: 题型:
将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500mL2mol/LNaOH溶液完全吸收,生成NaNO3和k*s*5*uNaNO2的混合溶液,其中生成的NaNO3的物质的量为( )
已知NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH= NaNO3+NaNO2+H2O,
A、0.2mol B、0.4mol C、0.6mol D、0.8mol
查看答案和解析>>
科目: 来源: 题型:
【化学与技术】
氯碱工业中曾用石棉隔膜电解槽来电解食盐水,下图即为石棉隔膜电解槽的示意图,回答下列问题:
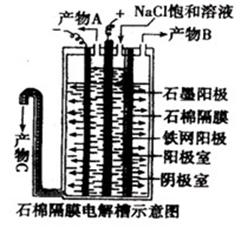
(1)产物A是 ;产物B是 ;产物C
(2)石棉隔膜能阻止 不能通过,但不能阻止 通过。
(3)粗盐水含Ca2+、Mg2+、SO42-等杂质离子,这些离子的存在除了会影响电解所得产品的纯度外,主要会 所以电解食盐水要求对粗盐水进行精制,请将精制时除去上述三种离子通常加入的化学试剂按加入的顺序依次写来 , 形成沉淀过滤后,还应加入盐酸调节pH,过滤所需要的玻璃仪器有
查看答案和解析>>
科目: 来源: 题型:
有机物A CH3CHClCH2OH,在一定条件下可以发生如下图所示的转化(其它产物和水已略去):
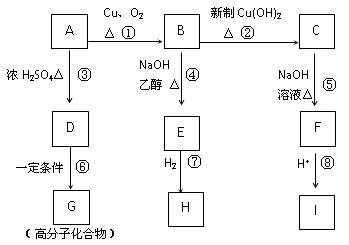
请回答下列问题:
(1)写出下列物质的结构简式:E ,I 。
(2)上述①~⑧的反应中, 是取代反应, 是消去反应(填编号)。
(3)写出下列反应的化学方程式:
A→B B→E ;D→G __
查看答案和解析>>
科目: 来源: 题型:
某些地区的水中可能含有少量下列盐类。当用新买来的铝锅或铝壶烧水时,遇到水的地方会变成黑色,据此可以判断此地下的水中含有
A.钠盐 B.钾盐 C.钙盐 D.铁盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com