
科目: 来源: 题型:
A是一种常见的单质,B、C为常见的化合物,A、B、C均含有元素x,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列说法中正确的是 ( )

A.X元素可能为铝
B.反应①和②互为可逆反应
C.X元素可能是金属,也可能是非金属
D.反应①和②一定为氧化还原反应
查看答案和解析>>
科目: 来源: 题型:阅读理解
某化学研究性学习小组讨论Fe3+和SO32—之间发生怎样的反应,提出了两种可能:
一是发生氧化还原反应:2Fe3++SO32—+H2O=2Fe2++SO42—+2H+;
二是发生双水解反应:2Fe3++3SO32—+6H2O=2Fe(OH)3(胶体)+3H2SO3。
为了证明是哪一种反应发生,同学们设计并实施了下列实验,请填写下列空白:
【实验Ⅰ】学生选择的实验用品:Na2SO3浓溶液、BaCl2稀溶液、稀盐酸;试管若干、胶头滴管若干。从选择的药品分析,作者设计这个实验的目的是 。
【实验Ⅱ】取5mLFeCl3浓溶液于试管中,逐滴加入Na2SO3浓溶液,观察到溶液颜色由黄色变为红棕色,无气泡产生,无沉淀生成,继续加入Na2SO3浓溶液至过量,溶液颜色加深,最终变为红褐色。这种红褐色“液体”是 ;向红褐色液体中逐滴加入稀盐酸至过量,可以观察到的现象是. ;
将溶液分成两等份,其中一份加入KSCN溶液,溶液变成血红色,另一份加入BaCl2稀溶液,有少量白色沉淀生成。产生血红色现象的离子方程式是 。
【实验Ⅲ】换用稀释的FeCl3和Na2SO3溶液重复实验,Ⅱ、Ⅲ产生的现象完全相同。由上述实验得出的结论是 ;
若在FeCl3浓溶液中加入Na2CO3浓溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是. 。
从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,分析其原因可能是:
① ;
② 。
查看答案和解析>>
科目: 来源: 题型:
已知如下两个热化学方程式:C(s)+O2(g)===CO2(g);△H==-393.5kJ/mol
2H2(g)+O2(g)===2H2O(g);△H===-483.6 kJ/mol。现有0.2mol炭粉和氢气组成的悬浮气体、固体混合物在氧气中完全燃烧,共放出63.53kJ热量。则炭粉与氢气的物质的量之比是
A.1:1 B. l:2 C.2:3 D.3:2
查看答案和解析>>
科目: 来源: 题型:
如下图是NaCl晶体的一个晶胞结构模型。KO2的晶体结构与NaCl相似,KO2可以看作是Na+的位置用K+代替,Cl-位置用O2-代替,则关于KO2晶体结构的描述正确的是
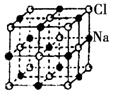
A.与K+距离相等且最近的O2-共有8个
B.与K+距离相等且最近的O2-构成的多面体是8面体
C.与K+距离相等且最近的K+有8个
D.一个KO2晶胞中摊得的K+和O2-粒子数均为6个
查看答案和解析>>
科目: 来源: 题型:
硝酸工业尾气中氮的氧化物(NO、NO2)是大气污染物,可用纯碱溶液吸收,有关的化学反应为:2NO2+Na2CO3 = NaNO2+NaNO3+CO2↑ ①
NO+NO2+Na2CO3 = 2NaNO2+CO2↑ ②
(1)若在标准状况下有NO、NO2的混合物恰好与50mL 1.0 mol·L-1的Na2CO3溶液反应完全,且生成NaNO2和NaNO3的物质的量的比值为4:1,则在混合气体中NO气体的体积分数为多少?
(2)设NO、NO2的混合气体用NOx表示,用纯碱溶液吸收,生成硝酸钠及亚硝酸钠再结晶分离。
①若该混合气体通入纯碱溶液时要求被完全吸收,则x的取值范围应为 。
②若生产每吨硝酸钠的成本为0.16万元,生产每吨亚硝酸钠的成本为0.27万元。目前市场出售价:硝酸钠每吨0.18万元,亚硝酸钠每吨0.28万元。则每处理22.4×106m3(标准状况)含NOx(x取值范围满足①中要求)体积分数为0.1%的尾气,求所得利润y(出售价减去成本价,单位:万元)与x的关系式。
查看答案和解析>>
科目: 来源: 题型:
如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于
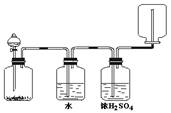
A.浓硫酸和乙醇反应制备乙烯
B.浓盐酸和二氧化锰反应制备氯气
C.碳酸钙和盐酸反应制备二氧化碳
D.锌和盐酸反应制备氢气
查看答案和解析>>
科目: 来源: 题型:
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ( )
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。
B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。
C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
D.氨气分子是极性分子而甲烷是非极性分子。
查看答案和解析>>
科目: 来源: 题型:
氯水的成分及探究
①新制氯水呈__ __色,或氯水能使淀粉碘化钾试纸变蓝,都可以说明___ ____存在
②氯水的PH值__ ___水,说明氯水呈___ _性
③向氯水中滴加紫色石蕊试液产生的现象是_____ ____,可以说明氯水中存在___ ___微粒
④在氯水中加入AgNO3溶液,产生的现象____ _____说明存在__ _____微粒
⑤可以用钢瓶来存在液氯,为了防止钢瓶的腐蚀,冲入氯气前必须_ ____
⑥在氯水中加入无水CuSO4固体,产生的现象____ _____说明存在__ ____微粒
查看答案和解析>>
科目: 来源: 题型:
下列物质的熔、沸点高低顺序正确的是 ( )
A.金刚石,晶体硅,二氧化硅,碳化硅B.CI4>CBr4>CCl4>CH4
C.MgO>Na2O>O2>N2 D.金刚石>生铁>纯铁>钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com