
科目: 来源: 题型:
已知蓝铜矿的主要成分是2CuCO3·Cu(OH)2,受热易分解。铝土矿的主要成分是Al2O3、Fe2O3、SiO2。经过一定条件的转化二者均可转化为金属单质,根据下列框图转化回答问题:
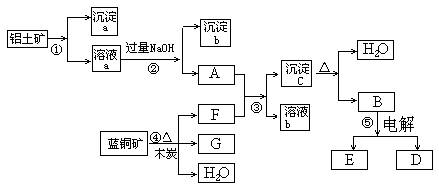
(1)写出①的离子方程式:______________________、_____________________。
(2)经过④、⑤步反应得到铜和金属铝,写出反应的化学方程式:
______________ _______、___________ ___________。
(3)若过量F与A反应,溶液b的成分是:__ ____(写化学式)。
查看答案和解析>>
科目: 来源: 题型:
下列离子组一定能大量共存的是( )
A.酚酞呈无色的溶液中:I-、CH3COO-、NO3-、Na+
B.甲基橙呈黄色的溶液中: Na+ 、CO32-、NO3-、NH4+
C.含大量Al3+的溶液中: K+、Na+、NO3- 、S2-
D.pH>7-的溶液中:CO32-、Cl-、F-、K+
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分,针对表中的①~⑧元素,填写下列空白:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①的气态氢化物分子的空间构型为__________ ________。
(2)②的气态氢化物稳定性比⑦的气态氢化物______ ___(填“强”、“弱”或“相同”)。
(3)由①与②形成的三原子分子的电子式为_________ ___ __________。
由③与⑧形成的离子化合物的电子式为__________ ____________。
(4)③、④、⑤离子半径依次_______ ____。(填“增大”、“减小”或“不变”)
(5)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物反应离子方程式为:
。
查看答案和解析>>
科目: 来源: 题型:
下列实验中,反应速率加快是由催化剂引起的是 ( )
A.在炭粉中加入KCl03,点燃时燃烧更为剧烈
B.H2O2中加入少量FeCl3,即可迅速放出气体
C.将炭块粉碎成粉末状,可使燃烧更加充分
D.锌与稀硫酸反应中加入少量硫酸铜,产生氢气速率加快
查看答案和解析>>
科目: 来源: 题型:
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是 ( )
A.X与Y形成化合物,X可以显负价,Y显正价
B.第一电离能可能Y小于X
C.气态氢化物的稳定性:HmY小于HnX
D.最高价含氧酸的酸性:X对应的酸性弱于于Y对应的
查看答案和解析>>
科目: 来源: 题型:
草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1 mol·L-1 KHC2O4溶液中,
下列关系不正确的是:
A.c(K+)+c(H+) = c(HC2O4-) + c(OH-) + 2 c(C2O42-)
B.c(HC2O4-) + c(C2O42-) = 0.1 mol·L-1K
C.c(C2O42-) > c(H2C2O4)
D.c(K+) = c(H2C2O4) + c(HC2O4-) + c(C2O42-)
查看答案和解析>>
科目: 来源: 题型:阅读理解
对于反应A(g)![]() 2B(g) DH>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示。回答下列各题。
2B(g) DH>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示。回答下列各题。

(1)根据曲线图,分析下列说法正确的是 ▲ (填字母) 。
A.a、c两点的反应速率:a 〉c
B.由状态b到状态a,可以通过加热的方法
C.b、c两点A气体的转化率相等
(2)上述反应在密闭容器(定容)中进行,达到平衡状态的标志是 ▲ (填字母) 。
A.单位时间内生成n mol A的同时分解2n molB
B.两种气体的体积分数不再改变
C.v正(A)=2v逆(B)
D.混合气体的密度不再发生变化
E.混合气体的压强不再发生变化
(3)若上述反应达平衡时,B气体的平衡浓度为0.1 mol·L-1 ,通过减小体积来增大体系的压强(温度保持不变),重新达平衡后,B气体的平衡浓度 ▲ 0.1 mol·L-1(填“〉”、“〈”或“=”) 。
(4)在100℃时,将0.40mol的B气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表的数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(B)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(A)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
① 在上述条件下,从反应开始至40s时,以A气体表示的该反应的平均反应速率为 ▲ ;
② 上表中n3 ▲ n4(填“〉”、“〈”或“=”),反应A(g)![]() 2B(g)在100℃时的平衡常数K的值为 ▲ ,升高温度后,反应2B(g)
2B(g)在100℃时的平衡常数K的值为 ▲ ,升高温度后,反应2B(g) ![]() A(g)的平衡常数K的值 ▲ (填“增大”、“减小”或“不变”);
A(g)的平衡常数K的值 ▲ (填“增大”、“减小”或“不变”);
③ 若在相同情况下最初向该容器中充入的是A气体,要达到上述同样的平衡状态,A气体的起始浓度为 ▲ mol·L-1 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com