
科目: 来源: 题型:
有一无色溶液,可能含有K+、A13+、Mg2+、NH4+、Cl—、SO42—、HCO3—、MnO4—中的几种。为确定其成分,做如下实验:①取部分溶液,加入适量Na2O2固体,产生无色无味的气体和白色沉淀,再加入足量的NaOH溶液后白色沉淀部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生。下列推断正确的
A.肯定有A13+、Mg2+、NH4+、Cl— B.肯定有Al3+、Mg2+、HCO3—
C.肯定有K+、HCO3—、MnO4— D.肯定有A13+、Mg2+、SO42—
查看答案和解析>>
科目: 来源: 题型:
一定温度下,在容积不变的密闭容器中发生反应:2NO2(g)![]() 2NO(g)+ O2(g),能说明该反应已达化学平衡状态的是
2NO(g)+ O2(g),能说明该反应已达化学平衡状态的是
①生成n mol O2的同时生成2n mol NO2
②生成n mol O2的同时生成2n mol NO
③容器内气体的压强不再改变 ④混合气体的颜色不再改变
⑤混合气体的密度不再改变
A. ①②④ B. ②③⑤ C. ①③④ D. ①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
下列溶液中的Cl-与50 mL 1 mol·L-1 AlCl3溶液中Cl-物质的量相等的是
A.150 mL 1 mol·L-1的NaCl溶液
B.75 mL 2 mol·L-1 NH4Cl溶液
C.75 mL 1 mol·L-1的FeCl3溶液
D.150 mL 2 mol·L-1的KCl溶液
查看答案和解析>>
科目: 来源: 题型:
“嫦娥二号”的制造使用了铝—锂、铝—镁等多种合金材料,火箭推进剂中发生反应:N2O4+2N2H4=3N2+4H2O。下列有关叙述不正确的是
A.锂、铝、镁都属于金属单质
B.火箭推进剂中发生的反应属于氧化还原反应
C.16 g N2H4中含有的H原子数为1.204×1023
D.N2O4属于氧化物
查看答案和解析>>
科目: 来源: 题型:
硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。
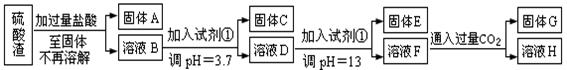
已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1。请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式: 。
(2)上述流程中两次使用试剂①,推测试剂①应该是 (填以下字母编号)
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(3)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是 ;(任写一点)
(4)H中溶质的化学式: ;
(5)计算溶液F中c(Mg2+)= ( 25℃时,氢氧化镁的Ksp=5.6×10-12)
查看答案和解析>>
科目: 来源: 题型:
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置。请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题。
供选择的药品:铜丝、稀硝酸、烧碱溶液、铁粉、CaCO3颗粒。

(一)实验步骤:
(1)实验开始时,必须进行的第一步操作是检验装置的 ;
(2)向试管中加入一定量的固体药品 ,其目的是 ;然后向试管中倒入过量的稀硝酸,并迅速塞紧带铜丝和导管的橡皮塞;
(3)反应一段时间后,用蘸有NaOH溶液的棉花团封住导管口;
(4)将铜丝向下移动插入试管液体中,使之与硝酸反应,反应的离子方程式是 ;
(5)将注射器插入试管口的橡皮塞中,向试管内推入空气,现象是
;
(二)问题探究:分别将等质量的铜片与等体积过量的浓、稀硝酸反应,所得溶液前者
呈绿色、后者呈蓝色,某同学认为可能是Cu2+浓度的差异引起的,你认为是否正确?
(填“正确”或“不正确”),理由是
查看答案和解析>>
科目: 来源: 题型:
由Cu、Cu2O、CuO组成的混合物,加入200mL 0.6mol/L的HNO3溶液恰好使混合物溶解,同时收集到448mL NO气体(标准状况)。求:
(1)若将等质量的上述混合物在加热条件下用H2全部还原,能生成多少克Cu?
(2)若题述混合物中含Cu 0.02mol,则其中含CuO多少mol ?
查看答案和解析>>
科目: 来源: 题型:
已知N2 (g) + 3H2(g) ![]() 2NH3(g) (正反应放热),工业合成氨采用在500℃的条件下进行的原因是
2NH3(g) (正反应放热),工业合成氨采用在500℃的条件下进行的原因是
① 只有在此温度下反应才能发生 ② 升高温度有利于NH3的合成
③ 提高反应速率,以提高单位时间内NH3的产量 ④ 使催化剂达到最佳催化活性
A.③④ B.①② C.①③ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com