
科目: 来源: 题型:
胶体燃料电池是电动车常用的四种蓄电池中的一种,该电池的总反应式为:
2PbSO4 + 2H2O ![]() Pb + PbO2 + 2H2SO4。下列说法正确的是
Pb + PbO2 + 2H2SO4。下列说法正确的是
A.胶体能发生电泳是由于胶体带电
B.放电时,Pb为负极,电极反应式为Pb- 2e?? = Pb2+
C.这种电池达到使用寿命之后可以随意丢弃,不会造成环境污染
D.利用这种电池电解精炼铜,当阴极析出0.64g铜时,该蓄电池中消耗H2SO4 0.02mol
查看答案和解析>>
科目: 来源: 题型:
已知:
![]()
(式中X代表卤素原子)有以下反应,最终产物是乙二酸。
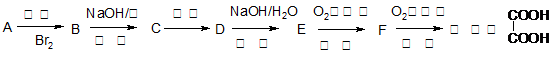
试回答下列问题:
(1)C的结构简式是 ;
(2)B→C的反应类型是 ;
(3)E→F的化学方程式是 ;
(4)写出E与乙二酸发生酯化反应生成环状化合物的化学方程式
;
(5)写出E与乙二酸反应生成高分子化合物的化学方程式
;
(6)由B发生水解反应或C发生水化反应均生成化合物G。在乙二酸、水、苯酚、G四种分子中,羟基上氢原子的活泼性由强到弱的顺序是 。
查看答案和解析>>
科目: 来源: 题型:
Ⅰ.玻璃棒是中学化学实验中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是
(填写编号)
①用pH试纸测定Na2CO3溶液的pH; ②配制一定物质的量浓度的氯化钠溶液; ③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体; ④探究Ba(OH)2![]() 8H2O晶体和NH4Cl晶体反应过程中的能量变化; ⑤用蒸馏法分离两种沸点差距较大的液体; ⑥过滤分离互不相溶的固体和液体; ⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程; ⑧稀释浓H2SO4的过程
8H2O晶体和NH4Cl晶体反应过程中的能量变化; ⑤用蒸馏法分离两种沸点差距较大的液体; ⑥过滤分离互不相溶的固体和液体; ⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程; ⑧稀释浓H2SO4的过程
Ⅱ.为测定某含有杂质Na2O的Na2O2样品的纯度,某小组同学分别设计了如下方案。
【方案一】准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na2O2的含量。
(1)此方案中,酸碱中和滴定时应选用指示剂是 。
【方案二】准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。

(2)该方案的实验过程中,仪器的连接顺序是 (填仪器下方序号),①中的进气口为 (填“A”或“B”)
(3)装置⑤的作用是 。
(4)在可供选用的反应物只有CaCO3固体,6mol/L盐酸和蒸馏水时,请设计一种最简单的测定Na2O2纯度的实验方案 。
查看答案和解析>>
科目: 来源: 题型:
在系统命名法中,下列烃的命名一定错误的是
A.2,2,3-三甲基-4-乙基己烷 B.2-甲基-3-乙基己烷
C.2-甲基-3-乙基戊烷 D.2-甲基-2-乙基庚烷
查看答案和解析>>
科目: 来源: 题型:
甲基丙烯酸甲酯是世界上年产量超过100万吨的高分子单体,旧法合成的反应是:
(CH3)2 C=O+HCN—→(CH3)2 C(OH)CN
(CH3)2C(OH)CN+CH3OH+H2SO4—→CH2=C(CH3)COOCH3+NH4HSO4
90年代新法的反应是: CH3C≡CH + CO + CH3OH![]() CH2=C(CH3)COOCH3
CH2=C(CH3)COOCH3
与旧法比较,新法的优点是
A.原料无爆炸危险 B.原料都是无毒物质
C.没有副产物,原料利用率高 D.产品性能更好
查看答案和解析>>
科目: 来源: 题型:
(I)多项选择题
CH3+、CH3-、CH3-都是重要的有机反应中间体,有关它们的说法正确的是 。
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个CH3-或一个CH3+和CH3-结合均可得到CH3CH3
(II)
锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的位置: 周期, 族, 区。
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式 ;葡萄糖分子中碳原子杂化方式有 。
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于 (填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在左下图中表示[Zn(NH3)4]2+中Zn2+与N之间的化学键。

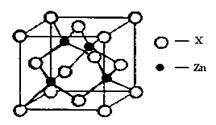
(4)右上图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为 ;该化合物的晶体熔点比干冰高得多,原因是 。
查看答案和解析>>
科目: 来源: 题型:
(共6分,每空1分)用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如下表所示。
| 实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
| 1 | 25.00 | 26.40 |
| 2 | 25.00 | 24.38 |
| 3 | 25.00 | 24.42 |
试回答下列问题:
(1)使用酚酞做指示剂,滴定过程中两眼应该注视_________________,滴定终点的判断是 。
(2)实验中,指示剂加2滴不能多加是因为:
(3)未知浓度的NaOH溶液的物质的量浓度为 mol/L。(精确到0.0001)
(4)有下列错误操作:
①酸式滴定管用蒸馏水洗净后,未经标准溶液润洗就注入标准的盐酸溶液
②用碱式滴定管取用待测液前,尖嘴部分有气泡,取用过程中气泡消失
③滴定前,读取酸液体积时视线低于酸式滴定管的液面,滴定后读出酸液的体积时,
视线高于酸式滴定管的液面
④锥形瓶用待测液润洗两次
哪些错误操作会使NaOH浓度的测定值偏低?答:_____________。
哪些错误操作会使NaOH浓度的测定值偏高?答:_____________。
查看答案和解析>>
科目: 来源: 题型:
下列各组离子一定能大量共存的是 ( )
A.含有大量Fe3+的溶液中:NH4+、Na+、![]() 、
、![]()
B.在强碱溶液中:Na+、K+、![]() 、
、![]() -
-
C.在c(H+)= 10-13mo1/L的溶液中:NH4+、A13+、![]() 、
、![]()
D.在pH=1的溶液中:K+、Fe2+、![]() 、
、![]()
查看答案和解析>>
科目: 来源: 题型:
右图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是

A.a为负极、b为正极 B.a为阳极、b为阴极
C.电解过程中,d电极质量增加 D.电解过程中,氯离子浓度不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com