
科目: 来源: 题型:
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是
A.元素A、B组成的化合物常温下一定呈气态
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
C.工业上常用电解法制备元素C、D、E的单质
D.化合物AE与CE古有相同类型的化学键
查看答案和解析>>
科目: 来源: 题型:
25
由短周期元素组成的化合物X是某抗酸药的有效成分。甲同学欲探究X的组成。
查阅资料:①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、磷酸铝、碱式碳酸镁铝。
②Al3+在pH=5.0时沉淀完全;
Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全。
实验过程:
Ⅰ.向化合物X粉末中加入过量盐酸,产生气体A,得到无色溶液。
Ⅱ.用铂丝蘸取少量I中所得的溶液,在火焰上灼烧,无黄色火焰。
Ⅲ.向I中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤。
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解。
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C。
Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是__________。
由Ⅰ、Ⅱ判断X一定不含有的元素是磷、_____________。
Ⅲ中生成B的离子方程式是_____________。
Ⅳ中B溶解的离子方程式是_____________。
沉淀C的化学式是_____________。
若上述n(A):n(B):n(C)=1:2:3,则X的化学式是_____________。
查看答案和解析>>
科目: 来源: 题型:
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·x H2O,经过滤、水洗除去其中的Cl,再烘干、焙烧除去水分得到粉体TiO2 。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
⑴ TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________。
⑵ 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
⑶ 下列可用于测定TiO2粒子大小的方法是_____________________(填字母代号)。
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
⑷ 配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是_________________;使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的_____(填字母代号)。
![]()
![]()
![]()
![]()
![]()
a b c d e
⑸ 滴定终点的现象是___________________________________________________。
⑹ 滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为_________________________。
⑺ 判断下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
① 若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果_________________________。
② 若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果_________。
查看答案和解析>>
科目: 来源: 题型:
某同学想通过比较两种最高价氧化物对应水化物的酸性强弱来验证硫与碳的非金属性的强弱,他采用了如图所示的装置。请回答:
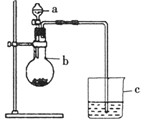
(1)仪器a的名称是 ,应盛放下列药品中的 。
A.稀硫酸 B.亚硫酸
C.氢硫酸 D.盐酸
(2)仪器b的名称是 ,应盛放下列药品中的 。
A.碳酸钙 B.硫酸钠
C.氯化钠 D.碳酸钠
(3)如果观察到C中的现象为 ,即可证明硫与碳的非金属性的强弱。
查看答案和解析>>
科目: 来源: 题型:
烯烃中碳碳双键是重要的官能团,在不同条件下能发生多种变化。
(1)烯烃的复分解反应就是两种烯烃交换双键两端的基团,生成两种新烯烃的反应。请写出在催化剂作用下,两个丙烯分子间发生复分解反应的化学方程式 。
(2)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的对应关系:
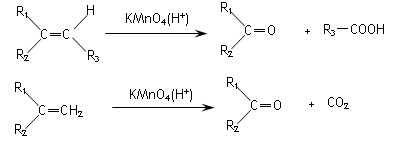
已知某烯烃的化学式为C5 H10 ,它与酸性高锰酸钾溶液反应后得到的产物若为乙酸和丙酸,则此烯烃的结构简式是 ;若为二氧化碳和丁酮( ),则此烯烃的结构简式是 。
查看答案和解析>>
科目: 来源: 题型:
下列判断中一定正确的是( )
A.CaCl2及CaO2固体中阴、阳离子数之比均为2∶1
B.等质量的O2与O3中,氧原子的个数比为3∶2
C.分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1∶2
D.10mL 0.3mol·L-1NaCl与30mL0.1mol·L-1AlCl3溶液中Cl-物质的量浓度比为1∶3
查看答案和解析>>
科目: 来源: 题型:
在由5种基团叫-CH3、-OH、-CHO、-C6H5、-COOH两两组成的物质中,能与NaOH溶液发生中和反应的有( ).
A.4种 B.5种 C.6种 D.7种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com