
科目: 来源: 题型:
某烷烃的结构为:![]() ,下列命名正确的是 ()
,下列命名正确的是 ()
A.1,2,4-三甲基-3-乙基戊烷 B.3-乙基-2,4-二甲基己烷
C.3,5-二甲基-4-乙基己烷 D.2,4-二甲基-3-乙基己烷
查看答案和解析>>
科目: 来源: 题型:
2002年诺贝尔化学奖表彰了两项成果,其中一项是瑞士科学家库尔特·维特里希发明了“利用核磁共振技术测定溶液中生物大分子三维结构的方法”。在化学上经常使用的是氢核磁共振谱,它是根据不同化学环境的氢原子在氢核磁共振谱中给出的信号不同来确定有机物分子中的不同的氢原子。下列有机物分子在核磁共振氢谱中只给出一种信号的是 ( )
A.HCHO B.CH3OH C.HCOOH D.CH3COOCH3
查看答案和解析>>
科目: 来源: 题型:
在3BrF3 +5H2O==HBrO3+Br2 +9HF+O2反应中,若有15mol H2O作还原剂,则被水还原的BrF3的物质的量为 ( )
A.6 mol B.12mol C. 4mol D.10 mol
查看答案和解析>>
科目: 来源: 题型:
现有钠、镁、铝各1mol,分别与100mL 5.0mol/L盐酸充分反应后,所得同温、同
压下的H2体积关系正确的是
A.产生H2体积相等 B.铝产生H2最多,钠产生H2最少
C.钠产生H2最多,铝产生H2最少 D.钠产生H2最多,镁、铝产生H2相等
查看答案和解析>>
科目: 来源: 题型:
下列有关0.2mol·L-1 BaCl2溶液的说法不正确的是
A.500mL溶液中Cl-离子浓度为0.2mol·L-
B.500mL溶液中Ba2+离子浓度为0.2mol·L-
C.500mL溶液中Cl-离子总数为0.2NA
D.500mL溶液中Ba2+和Cl-离子总数为0.6NA
查看答案和解析>>
科目: 来源: 题型:
实验室为了制得少量漂白粉,常用浓盐酸与二氧化锰先制取氯气,再用氯气与消石灰反应。已知氯气与氢氧化钙制漂白粉是放热反应[2Cl2+2Ca(OH)2![]() Ca(ClO)2+CaCl2+2H2O(反应放热)],温度稍高即会发生副反应6Cl2+6Ca(OH)2
Ca(ClO)2+CaCl2+2H2O(反应放热)],温度稍高即会发生副反应6Cl2+6Ca(OH)2![]() Ca(ClO3)2+5CaCl2+6H2O。现有甲、乙、丙三套装置(U形管中放有玻璃纤维,可使气体顺利通过)。
Ca(ClO3)2+5CaCl2+6H2O。现有甲、乙、丙三套装置(U形管中放有玻璃纤维,可使气体顺利通过)。

(1)请对三套装置的优缺点进行评价,并将选项序号填于下表内。a.容易引起环境污染
b.可防止环境污染 c.可防止副反应发生 d.易发生副反应 e.易控制反应速率 f.不易控制反应速率
| 优点 | 缺点 | |
| 甲装置 | ||
| 乙装置 | ||
| 丙装置 |
(2)请从甲、乙、丙三套装置中,选取合理的组成部分(A、B、C、D、E、F、G)组装一套你认为更完整的实验装置,则连接顺序为(按气流从左到右方向) 。
(3)在你所设计的装置及以上甲、乙、丙装置中,是否还缺少其他必要的装置,说明原因: 。
查看答案和解析>>
科目: 来源: 题型:
实验一:某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案。装置如图:
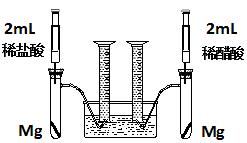
实验方案:在两试管中分别加入过量镁条,同时将两注射器中的溶液注入相应试管中,观察产生氢气的速率和体积。
(1)盐酸与镁反应的离子方程式为 。
(2)在上述实验方案中有一明显欠缺,该欠缺是 。
(3)在欠缺已经改正的方案下,反应起始时,产生氢气的速率关系应是 ;最终产生氢气的体积关系应是 。
(4)实验中产生的氢气体积比理论值高,可能原因是 。
(5)通过比较起始反应的速率可以得出的结论是 。
(6)除上述方法外,还可以通过其他方法比较盐酸和醋酸的酸性,请写出其中一种更简单的方法
。
实验二:某二元酸(H2B)在水中的电离方程式是: H2B=H++HB- HB-![]() H++B2-
H++B2-
回答下列问题:
(1)请判断H2B是强电解质还是弱电解质?
(2)已知0.1mol·L-1 NaHB溶液的pH=2,则0.1mol·L-1 H2B溶液中氢离子的物质的量浓度应 0.11 mol·L-1(填“<”,“>”或“=”)
(3)在0.1mol/L的Na2B溶液中,下列离子浓度关系式正确的是_______。
A.c(H+)+c(HB-)+c(H2B)=0.1mol/L B.c(Na+)+c(OH-)=c(H+)+ c(HB-)
C.c(Na+)+ c(H+)= c(OH-)+ c(HB-)+2c(B2-) D.c(Na+)=2c(B2-)+2 c(HB-)
(4)0.1mol/LNaHB溶液中各种离子浓度由大到小的顺序是_______________________。
查看答案和解析>>
科目: 来源: 题型:
已知高锰酸钾与重铬酸钾(K2Cr2O7)都是化学中常用的强氧化剂,高锰酸钾溶液呈紫红色而重铬酸钾溶液中存在如下平衡:
2CrO42—(黄色)+2H + ![]() Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
若要使溶液的橙色加深,下列可采用的方法是
A.加入适量稀盐酸 B.加入适量稀硝酸
C.加入适量烧碱固体 D.加水稀释
查看答案和解析>>
科目: 来源: 题型:
电解法制烧碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42- 杂质,不符合电解要求,因此必须经过精制。某校实验小组精制粗盐水的实验过程如下:
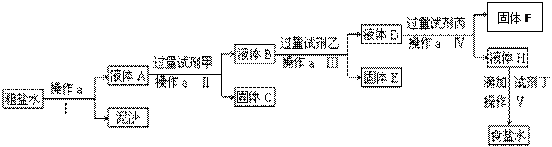
请回答以下问题:
(1)操作a的名称是____________。
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的沉淀,则试剂甲为________溶液。试剂乙为 ,固体F为 。
(3)在第Ⅴ步中,加入试剂丁直到溶液无明显变化时,写出此过程的化学方程式 、 _ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com