
科目: 来源: 题型:
下列离子方程式书写不正确的是
A.AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时,
2Al3+ + 7OH- = Al(OH)3↓+ AlO2- + 2H2O
B.Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,
2Fe2+ + 4Br- +3Cl2 = 2 Fe3+ + 2Br2 + 6Cl-
C.CuCl2溶液与NaHS溶液反应,当n(CuCl2):n(NaHS)=1:2时
Cu2++2HS-= CuS↓+2H2S↑
D.Fe与稀硝酸反应,当n(Fe):n(HNO3)=1:2时,
3 Fe +2NO3- +8H+ = 3 Fe2+ +2NO↑+4H2O
查看答案和解析>>
科目: 来源: 题型:
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。
(1)实验时,为在E烧瓶中收集到NO,以便观察颜色,必须事先除去其中的空气。其中第一步实验操作为: ___________。如何确定E中空气已被赶尽: ____________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的离子反应方程式为 。
(3)如何证明E中收集到的是NO而不是H2? 。
一段时间后,C中白色沉淀溶解,其原因是______________________ ____。
(4)装置D的作用是__________________________________________________。

查看答案和解析>>
科目: 来源: 题型:
下列电离方程式正确的是 ( )
A.H3PO4![]() 3H+ + PO43- B.CaCO3
3H+ + PO43- B.CaCO3![]() Ca2+ + CO32-
Ca2+ + CO32-
C.NaHS![]() Na+ + H+ + S2- D. Al(OH)3
Na+ + H+ + S2- D. Al(OH)3![]() H2O + AlO2- + H+
H2O + AlO2- + H+
查看答案和解析>>
科目: 来源: 题型:
用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象可得出两条有关过氧化钠跟水反应的结论是:
第一: ;第二: 。
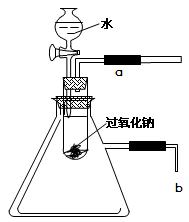
(2)某研究性学习小组拟用如下图所示的装置进行实验,
以验证上述结论。
用以验证第一条结论的实验操作是 现象是 。
为了验证第二条结论,将管口b浸入水中,可观察到的现象为 。
查看答案和解析>>
科目: 来源: 题型:
如图所示,△H1=-393.5 kJ·mol-1,△H2=-395.4 kJ·mol-1,下列说法或表示中,正确的是

A. C(s、石墨)== C(s、金刚石) △H= +1.9 kJ??mol-1
B. 石墨和金刚石的转化是物理变化
C. 石墨的稳定性比金刚石弱
D. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
查看答案和解析>>
科目: 来源: 题型:
在0.1mol·L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH ![]() CH3COO-+H+,对于该平衡,下列叙述中,正确的是
CH3COO-+H+,对于该平衡,下列叙述中,正确的是
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol·L-1 HCl溶液,溶液中[ H+] 减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2 (g) +2H2O(g) △H1=- 574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=—1160kJ·mol-1
下到选项正确的是 ( )
A.CH4 (g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=- 867kJ·mol-1
B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)的反应热为△H3,
则△H3>△H1
C.若用0.2molCH4还原NO2至N2,则反应中放出的热量一定为173.4kJ
D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为1.6mol
查看答案和解析>>
科目: 来源: 题型:
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO): CO(g)+2H2(g) ![]() CH3OH(g),根据题意完成下列各题:
CH3OH(g),根据题意完成下列各题:

(1)合成甲醇反应中,其反应热△H 0(填“>”“<”“=”)
(2)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2 下列有关该体系的说法正确的是
a. 氢气的浓度减少
b. 正反应速率加快,逆反应速率也加快
c. 甲醇的物质的量增加
d. 重新平衡时n(H2)/n(CH3OH)增大
(3)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: (用化学方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
在相同温度时,100mL0.01mol??L-1的醋酸溶液与10mL 0.1mol??L-1的醋酸溶液相比较,下列数值中,前者大于后者的是
A. H+的物质的量 B. 醋酸的电离常数
C. 中和时所需NaOH的量 D. CH3COOH的物质的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com