
科目: 来源: 题型:
在下列物质中(填序号)
(A)Cl2 (B)NaI (C)H2S (D)CO2 (E)CaCl2 (F)N2
(G)CCl4 (H)Na2O (I)NH3 (J)HBr
(1)含离子键的物质是____________;
(2)含有共价键化合物的是_____________________;
(3)由极性键形成的非极性分子是_______________;
(4)由非极性键形成的非极性分子是_______________。
查看答案和解析>>
科目: 来源: 题型:
用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是
A.直线形;三角锥形 B. V形;三角锥形
C.直线形;平面三角形 D. V形;平面三角形
查看答案和解析>>
科目: 来源: 题型:
茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案用以测定某品牌茶叶中钙元素的质量分数并检验铁元素的存在(已知![]() 为白色沉淀物质)。首先取200g茶叶样品焙烧得灰粉后进行如下操作:
为白色沉淀物质)。首先取200g茶叶样品焙烧得灰粉后进行如下操作:
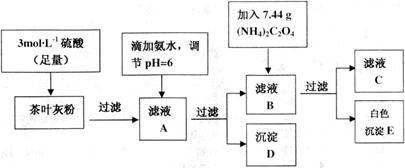
请回答下列有关问题:
(1)文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为::
| 离子 |
|
|
| 完全沉淀时的pH | 13 | 4.1 |
实验前要先将茶叶样品高温灼烧成灰粉,其主要目的是__________。
(2)写出从滤液A→沉淀D的离子反应方程式__________。
(3)为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,试
判断沉淀D已经洗涤干净的方法是__________。
(4)用KMnO![]() 标准溶液滴定C溶液时所发生的反应为:
标准溶液滴定C溶液时所发生的反应为:
![]() 。
。
现将滤液C稀释至500 mL,再取其中的25.00 mL溶液,用硫酸酸化后,用0.1000
mol·L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液10.00 mL。
①此步操作过程中需要用到下列哪些仪器(填写序号)________;
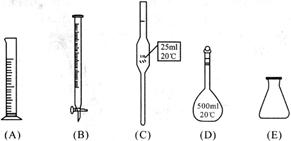
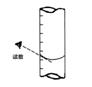
②达到滴定终点时,溶液的颜色变化是________;
③滴定到终点,静置后,如右图读取KMnO4标准溶液的刻度数据,则测定的钙元素含量将________ (填“偏高”、“偏低”、“无影响”)。
(5)原茶叶中钙元素的质量分数为________。
(6)可以通过检验滤液A来验证该品牌茶叶中是否含有铁元素,所加试剂及实验现象是________。
查看答案和解析>>
科目: 来源: 题型:
元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是
A.同周期元素中Y的非金属性最强 B.原子半径X>Y,离子半径X+>Z2-
C.同族元素中Z的氢化物稳定性最强 D.同周期元素中Y的氢化物水溶液酸性最强
查看答案和解析>>
科目: 来源: 题型:
下列有关实验的说法正确的是
A.蓝瓶子实验中,一定要在碱性条件且葡萄糖作氧化剂,且亚甲基蓝的化学振荡可以无限次重复
B.在氯气的生成及其性质的检验微型实验中,用氯酸钾和浓盐酸制取3molCl2时转移6mol电子
C.水的电解与氢氧混合气爆鸣的微型实验中,也可用稀盐酸溶液代替5% NaOH溶液增强导电性
D.电浮选凝聚法污水处理实验中,一方面利用Fe(OH)3具有吸附性,另一方面利用产生的气泡把污水中的悬浮物带到水面形成浮渣层
查看答案和解析>>
科目: 来源: 题型:
某温度下,将Cl2通入NaOH 溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定,ClO-与ClO3-的浓度之比为1:3,则反应中,被还原的氯元素与被氧化的氯元素物质的量之比为
A. 21:5 B. 11:3 C. 3:1 D. 4:1
查看答案和解析>>
科目: 来源: 题型:
下列关于氯水的叙述中,正确的是
A.久置的氯水中已没有分子,只有离子
B.新制氯水在光照的条件下,可以产生气体,该气体是氯气
C.新制氯水中滴加硝酸银溶液,没有任何现象
D.新制氯水可以使干燥的布条褪色
查看答案和解析>>
科目: 来源: 题型:
下图为物质A~I的转化关系(部分反应物、生成物没有列出)。其中B为某金属矿的主要成分,经过一系列反应可得到E和F。D、E常温下为气体,D、F为常见单质,单质F可与H的浓溶液加热时发生反应。
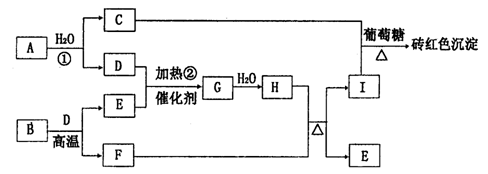
请回答下列问题:
(1)写出G的化学式:________________。
(2)反应①的离子方程式为__________________。
(3)单质F与H的浓溶液发生反应的化学方程式为______________________。
(4)用Pt作电极电解I溶液,完全电解后的电解质溶液是_______________,其阳极的电极反应式为____________________。
(5)已知每16gE与D完全反应,放出24.75 kJ热量,则反应②的热化学方程式为
________________________________________________.
(6)工业制备G时,混合气体的组成中E占7%、D占11%,现有100体积混合气体进入反应装置,导出的气体恢复到原温度和压强后变为97.2体积。则E的转化率为________.
查看答案和解析>>
科目: 来源: 题型:
将Cu与CuO的混合物20.8g加入到50mL 18.4mol/L浓H2SO4中,加热充分反应至固体物质完全溶解,冷却后将混合液稀释至1000 mL,测得c(Cu2+)=0.3 mol/L。试计算:(本题无计算过程不给分)
(1)反应过程中放出的气体在标准状况下的体积(不考虑气体在溶液中的溶解)。
(2)溶液稀释后,c(H+)是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com