
科目: 来源: 题型:
如图所示,在一个小烧杯里加入研细的20g Ba(OH)2·8H2O晶体。将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入10g NH4Cl晶体,并用玻璃棒快速搅拌。
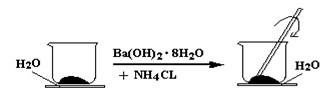
![]() (1)实验中要用玻璃棒搅拌的原因是
(1)实验中要用玻璃棒搅拌的原因是
![]() (2)写出有关反应的化学方程式: ,
(2)写出有关反应的化学方程式: ,
该反应 (填“是”或“不是”)氧化还原反应。w.w.w.k.&s.5*u.c.#om
(3)该实验中观察到的现象除产生刺激性气味的气体及反应混合物呈糊状以外,还有
![]() 。
。
(4)通过最后一个现象可以说明该反应为_________(填“吸”或“放”)热反应,这是由于反应物的总能量_________(填“大于”或“小于”)生成物的总能量。
查看答案和解析>>
科目: 来源: 题型:
把A、B、C、D4块金属片浸入稀硫酸中,用导线两两相连组成原电池。若A、B相连时,A为负极;C、D相连时,D上产生大量气泡;A、C相连时,电流由C经导线流向A;B、D相连时,电子由D经导线流向B,则此4种金属的活动性由强到弱的顺序为( )
A>B>C>D B. A>C>D>B C C>A>B>D D. B>A>C>D
查看答案和解析>>
科目: 来源: 题型:
下列说法中,可以证明反应N2+3H2 ![]() 2NH3已达到平衡状态的是 :
2NH3已达到平衡状态的是 :
A.1个N≡N键断裂的同时,有3个N–H键形成
B.1个N≡N键断裂的同时,有3个H–H键断裂
C.1个N≡N键断裂的同时,有6个N–H键断裂
D.1个N≡N键断裂的同时,有6个N–H键形成
查看答案和解析>>
科目: 来源: 题型:
(本小题12分) A、B、C、D、E是五种短周期元素,原子序数依次增大。前五种的原子序数之和是E的原子序数的二倍。E的阳离子与D的阴离子都比A阳离子多2个电子层。D与五种元素中任意一种都可形成原子个数比不相同的若干种化合物。B是形成化合物种类最多的元素。请回答下列问题:
(1)写出元素符号:A________,E________。
(2)D在周期表中位于第_______周期第________族。
(3)五种元素原子半径由大到小的顺序是(用A~E字母表示)_______________。
(4)A、B、C、D可形成一种受热易分解的化合物,写出该化合物受热分解的化学方程式____________________________________________________________。
(5)A、B、D可形成A2B2D4型化合物,该化合物的名称是_____________。
查看答案和解析>>
科目: 来源: 题型:
下列表达正确的是( )
A.氧族元素包括氧、硫、锡、碲、钋 ![]() Na2O2固体中的阳离k*s^5#u子和阴离k*s^5#u子个数比为1:1
Na2O2固体中的阳离k*s^5#u子和阴离k*s^5#u子个数比为1:1
C.H、D、T、H+可以用来表示氢元素的四种同位素
D.表示金属元素名称的汉字不一定都含“钅”旁
查看答案和解析>>
科目: 来源: 题型:
25℃时,氢氧化钠的溶解度为40 g,向100 g 水中投入一定量金属钠,反应完全后,恢复至25℃,此时溶液恰好处于饱和状态且无晶体析出,则投入的钠的质量约为( )
A.23.5 g ![]() 11.5 g C.19.5 g D. 23.0 g
11.5 g C.19.5 g D. 23.0 g
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D均为短周期元素,原子序数依次增大。已知:
①A与D同主族,A形成的氢化物分子M与D形成的氢化物分子N都含有18个电子;
②一定条件下,A、D分别和B形成的化合物X和Y具有相同的摩尔质量,且焰色反应均呈黄色;
③A和C形成的化合物Z可形成原子晶体。
请回答下列问题:
(1)X的电子式为_____________;Z的化学式为______________。
(2)A、B、C、D四种元素的原子半径按由小到大排列的顺序为: _______________________________________________(用元素符号表示)。
(3)化合物Y的水溶液pH>7,用离子方程式说明原因: 。
(4)在M的溶液中通入N,可发生反应生成D的单质和A的另一种氢化物,试写出化学方程式____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
物质的分类依据通常有组成和性质,下列对钠的化合物的分类的说法中,只考虑组成的是( )
A.Na2O2是氧化物,不是碱性氧化物
B.Na2CO3不是碱,是一种钠盐
C.NaOH是一元碱、强碱
D.NaClO是氧化性盐、含氧酸盐
查看答案和解析>>
科目: 来源: 题型:
天然气燃烧不完全会产生有毒气体CO,又知CO和CH4燃烧的热化学方程式分别为
2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890 kJ·mol-1
又知由H2与O2反应生成液态H2O 比生成气态H2O 多放出44 kJ·mol-1的热量。则下列热化学方程式正确的是 ( )
A.2CH4(g)+O2(g)=CO2(g)+CO(g)+4H2O(l) ΔH=-1214 kJ·mol-1
B.2CH4(g)+O2(g)=CO2(g)+CO(g)+4H2O(g) ΔH=-1038 kJ·mol-1
C.3CH4(g)+5O2(g)=CO2(g)+2CO(g)+6H2O(l) ΔH=-1538 kJ·mol-1
D.3CH4(g)+5O2(g)=CO2(g)+2CO(g)+6H2O(g) ΔH=-1840 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com