
科目: 来源: 题型:
巴豆酸的结构简式为CH3-CH=CH-COOH,现有
①溴水 ②氢氧化钠溶液 ③2-丙醇 ④酸化的高锰酸钾溶液。
试根据其结构特点判断在一定条件下能与巴豆酸反应的物质组合是
A.①④ B.①③④ C.②③ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结构如右图,下列关于该物质的说法正确的是
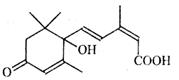
A.其分子式为C15H22O4
B.1 mol该物质与NaOH溶液反应,最多消耗2 molNaOH
C.既能发生加聚反应,又能发生缩聚反应
D.既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色
查看答案和解析>>
科目: 来源: 题型:
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示。则下列说法正确的是

A.构成原电池时b极反应为: Cu﹣2e-=Cu2+
B.构成电解池时a极质量一定减少
C.构成电解池时b 极质量可能减少也可能增加
D.构成的原电池或电解池工作后就可能产生大量气体
查看答案和解析>>
科目: 来源: 题型:
铜的冶炼过程大致可分为:①富集,将硫化物矿进行浮选;②焙烧,主要反应为
2CuFeS2+4O2 == Cu2S+3SO2+2FeO(炉渣);③制粗铜,在1200℃发生的主要反应为: 2Cu2S+3O2 == 2Cu2O+2SO2;2Cu2O+Cu2S == 6Cu+SO2↑;④电解精炼铜。下列说法不正确的是( )
A.Cu2O是红色固体
B.冶炼过程中的尾气可用来制硫酸
C.上述过程中,由2 mol CuFeS2制取Cu时,最少消耗5.0mol O2
D.电解精炼铜的开始阶段,每转移2mol电子时,阳极溶解铜的质量为64g
查看答案和解析>>
科目: 来源: 题型:
按要求进行书写:
(1)氯化钡的电离方程式:___________
(2)氢氧化亚铁在空气中被氧化的化学方程式:___________
(3)过氧化钠与水反应的化学方程式:___________
(4)在化学方程式上用双线桥法表示电子转移的方向及数目:
MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
查看答案和解析>>
科目: 来源: 题型:
2008年10月8日,美籍华裔科学家钱永健获得2008年度诺贝尔化学奖。16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获“美国西屋科学天才奖”。下列叙述正确的是
A.金属腐蚀就是金属失去电子被还原的过程
B.将水库中的水闸(钢板)与外加直流电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀
C.合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其成分金属强
D.铜板上的铁铆钉处在潮湿的空气中直接发生反应:Fe-3e- = Fe3+,继而形成铁锈
查看答案和解析>>
科目: 来源: 题型:阅读理解
海水中化学资源的综合开发利用已受到各国的高度重视。Br2和Mg等两种单质都可以从海水中提取,下图为提取它们的步骤:

请回答:
I.从海水中提取的溴占世界年产量的1/3,主要方法就是上述流程中的空气吹出法。
(1)制取Br2时,第一次通入Cl2发生反应的离子方程式是__________________。
(2)吸收塔中反应的离子方程式是________________________________________。
由(1)、(2)可知,SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
__________________。( 用“”表示)
II.镁及其合金是用途很广泛的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用___________(写化学式)。
(2)加入试剂②后反应泊离子方程式是_________________________________。
(3)步骤①包括加热、蒸发、冷却、结晶、_________。
(4)通电时无水MgCl2在熔融状态下反应的化学方程式是
___________________________________________________。
III.上述流程在生产溴和镁的同时还可以制得其他化工物质,比如制备耐火材料氧化镁和盐酸。生产方法是:
①将氯化镁晶体(MgCl2·6H2O)加热到523OC以上,该晶体可以分解得到耐火材料氧化镁和两种气态化合物,其中一种气体常温下为无色液体。
②将两种气体冷却到室温,再根据需要,加入不同量的水,就可得到不同浓度的盐酸。
(1)MgCl2·6H2O在523OC以上分解的化学方程式是_____________________________。
(2)现用1mol MgCl2·6H2O分解所得的非固体产物来制取密度为1.19g/cm3的盐酸溶液168mL,需加水__________g(精确到0.1),该盐酸中溶质的物质的量浓度是____________mol/L(精确到0.1)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com