
科目: 来源: 题型:
下列有关离子的检验中,结论正确的是 ( )
A.向某溶液中加入足量盐酸,产生无色无味气体,则该溶液中一定含有CO32-
B.向某溶液中加入足量氨水,产生白色沉淀,则该溶液中一定含有Al3+
C.向某溶液中加入足量盐酸,最终得到无色溶液,则该溶液中可能含有AlO2-
D.向某溶液中加入Na2CO3溶液,产生白色沉淀,则该溶液中一定含有Ca2
查看答案和解析>>
科目: 来源: 题型:
以下有关金属钠说法正确的是
A.金属钠很容易被空气中的氧气氧化,故金属钠的保存通常用水封
B. Na2O 、Na2O2均为碱性氧化物
C. 将金属钠放入FeCl3溶液中会有红褐色沉淀产生
D. 金属钠切开,表面很快变暗,故Na2O是灰黑色的
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250![]() 0.2
0.2![]() 的醋酸溶液,用0.2
的醋酸溶液,用0.2![]() 的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250![]() 0.2
0.2![]() 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、
醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、
。
(2)为标定某醋酸溶液的准确浓度,用0.2000![]() 的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
则该醋酸溶液的准确浓度为 ![]() 。(保留小数点后四位)
。(保留小数点后四位)
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,结果如下:
| 醋酸浓度 (mol·L–1) | 0.00l0 | 0.0100 | 0.0200 | 0.1000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 |
回答下列问题:
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是
。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度 。(填“增大”、“减小”或“不变”)
实验三 探究温度对醋酸电离程度的影响
(5)请你设计一个实验完成该探究,请简述你的实验方案
。
查看答案和解析>>
科目: 来源: 题型:
已知HCN(aq)与NaOH(aq)反应的![]() ;HCl(aq)与NaOH(aq)反应的
;HCl(aq)与NaOH(aq)反应的![]() ,则HCN在水溶液中电离的
,则HCN在水溶液中电离的![]() 等于 ( )
等于 ( )
A.![]()
![]() B.-43.5
B.-43.5![]()
C.+43.5![]() D.+67.7
D.+67.7![]()
查看答案和解析>>
科目: 来源: 题型:
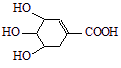 八角茴香含有一种抗亚洲禽流感病毒的重要成分——莽草酸,其分子结构如下图。下列关于莽草酸的说法错误的是
八角茴香含有一种抗亚洲禽流感病毒的重要成分——莽草酸,其分子结构如下图。下列关于莽草酸的说法错误的是
A.分子式为C7H10O5 B.遇FeCl3溶液呈紫色
C.能使溴水褪色 D.能溶于水
查看答案和解析>>
科目: 来源: 题型:
某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:3Cl2+6NaOH=5NaCl+NaClO3+3H2O),经测定ClO—与ClO3—的物质的量之比为1∶3,则氯气与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为
A.21∶5 B.11∶3 C.3∶1 D.4∶1
查看答案和解析>>
科目: 来源: 题型:
实验室用密度为1.18![]() ,质量分数为36.5%浓盐酸配制450
,质量分数为36.5%浓盐酸配制450![]() 0.1
0.1![]() 的盐酸溶液,填空并请回答下列问题:
的盐酸溶液,填空并请回答下列问题:
(1) 配制450![]() 0.1
0.1![]() 的盐酸溶液
的盐酸溶液
| 应量取盐酸体积/ | 应选用容量瓶的规格/ |
查看答案和解析>>
科目: 来源: 题型:
盐酸、硫酸和硝酸是中学阶段常见的三种强酸。请就三者与金属铜的反应情况,回答下列问题:
(1)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式 。
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是 ,反应中所消耗的硝酸的物质的量可能为 .
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解成蓝色溶液,该反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
Fe(OH)2在空气中极易被氧化,而使实验室制取存在一定困难,人们尝试用多种方法来制得白色的Fe(OH)2沉淀。

(1)方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
①配制FeSO4溶液时,在蒸馏水中加入硫酸亚铁晶体外还需加入 。
②除去蒸馏水中溶解的O2常采用 的方法。
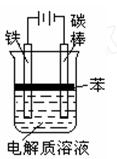
(2)方法二:用电解法制Fe(OH)2,实验装置如上左图所示。
①电解时,电解质溶液应选用下列试剂中的 (填编号字母)
A.氯化钠溶液 B.稀硫酸 C.硫酸铜溶液 D.碳酸钠溶液
②电解时阴极的电极反应为: 。
③电解质溶液液面复盖一层苯所起的作用是 。
(3)方法三:在如上图右装置,先打开止水夹,反应一段时间后关闭止水夹,右侧试管内可见到白色沉淀。
①该法可使沉淀的白色维持较长时间,其原因是 。
②该法操作不当,在右侧试管中得不到沉淀,其原因是 。
查看答案和解析>>
科目: 来源: 题型:
酸根离子RO![]() 所含电子数比硝酸根离子NO
所含电子数比硝酸根离子NO![]() 的电子数多10,则下列说法正确的是
的电子数多10,则下列说法正确的是
A.R和N为同周期元素
B.R和N是同主族元素
C.RO![]() 和NO
和NO![]() 只可能被还原,不可能被氧化
只可能被还原,不可能被氧化
D.RO![]() 中R元素与NO
中R元素与NO![]() 中N元素的化合价相同
中N元素的化合价相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com