
科目: 来源: 题型:
下列各组物质中,属于同分异构体的是
A.O2和O3
B.CH2=CHCH2CH3和CH3CH=CHCH3
C. CH3CH2OH和CH3OCH3
D. CH3CH2CH3和CH3(CH2)2CH3
查看答案和解析>>
科目: 来源: 题型:阅读理解
三氯化铬是化学合成中的常见物质,三氯化铬易升华,在高温下能被氧气氧化,碱性条件下能被H2O2氧化为Cr(Ⅵ)。制三氯化铬的流程如下:

(1)重铬酸铵分解产生的三氧化二铬(Cr2O3难溶于水)需用蒸馏水洗涤的原因 ▲ ,如何用简单方法判断其已洗涤干净 ▲ 。w ww.k s5u. co m
(2)已知CCl4沸点为57.6℃,为保证稳定的CCl4气流,适宜的加热方式是 ▲ 。
(3)用右图装置制备CrCl3时,主要步骤包括:①将产物收集到蒸发皿中;②加热反应管至400℃,开始向三颈烧瓶中通人氮气,使CCl4蒸气经氮气载入反应室进行反应,继续升温到650℃;③三颈烧瓶中装入150mLCCl4,并加热CCl4,温度控制在50~60℃之间;④反应管出口端出现了CrCl3升华物时,切断加热管式炉的电源;⑤停止加热CCl4,继续通人氮气;⑥检查装置气密性。正确的顺序为:⑥→③→
▲ 。

(4)已知反应管中发生的主要反应有:Cr2O3 + 3CCl4 → 2CrCl3 + 3COCl2,因光气剧毒,实验需在通风橱中进行,并用乙醇处理COCl2,生成一种含氧酸酯(C5H10O3),用乙醇处理尾气的化学方程式为 ▲ 。
(5)样品中三氯化铬质量分数的测定
称取样品0.3300g,加水溶解并定容于250mL容量瓶中。移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入1gNa2O2,充分加热煮沸,适当稀释,然后加入过量的2mol/LH2SO4至溶液呈强酸性,此时铬以Cr2O![]() 存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
已知:Cr2O![]() +6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2===Na2S4O6+2NaI。
+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2===Na2S4O6+2NaI。
①该实验可选用的指示剂名称为 ▲ 。w ww.k s5u. co m
②移入碘量瓶的CrCl3溶液需加热煮沸,加入Na2O2后也要加热煮沸,其主要原因是 ▲ 。
③样品中无水三氯化铬的质量分数为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
在反应5 NH4NO3![]() 2 HNO3 +4 N2↑+9 H2O 中,氧化产物与还原产物的物质的量之比为
2 HNO3 +4 N2↑+9 H2O 中,氧化产物与还原产物的物质的量之比为
A. 5∶3 B. 3∶5 C. 1∶1 D. 2∶1
查看答案和解析>>
科目: 来源: 题型:
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
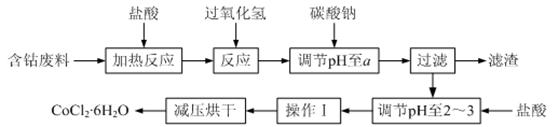
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
⑴在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为 ▲ 。
⑵加入碳酸钠调节pH至a,a的范围是 ▲ 。
⑶操作Ⅰ包含3个基本实验操作,它们是 ▲ 和过滤。
⑷制得的CoCl2·6H2O需减压烘干的原因是 ▲ 。
⑸为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 ▲ 。
⑹在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,采用的方法是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
用如图所示的装置进行实验,反应一段时间后断开K,向烧杯中加入0.1 mol CuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是( )
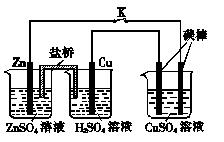
A.铜棒为正极,其电极反应式为2H++2e-===H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过电子的物质的量为0.2 mol
查看答案和解析>>
科目: 来源: 题型:
下列对分子结构叙述不正确的是( )
A.H2O2分子中,两个O之间形成1对共用电子对 B.N2的电子式是N┇┇N
C.CCl4和甲烷都是正四面体型分子 D.CO2和CS2都是直线型分子
查看答案和解析>>
科目: 来源: 题型:阅读理解
(I)人类的衣食住行都离不开化学,化学与生活密切相关。“民以食为天”,人类生命活动所需的各种营养素主要来自于食物。
| 主 食 | 米 饭 |
| 副 食 | 红烧鱼 |
| 饮 品 | 豆 浆 |
| 你的补充 | ? |
上表制定的食谱中,主食含有的营养素主要是________(选填“糖类”、“油脂”或“蛋白质”,下同),副食含有的营养素主要是________;豆浆所属的分散系为________(选填“溶液”、“浊液”或“胶体”)。考虑营养成分的均衡搭配,应增加的配菜是 。
(II)在我们的日常生活中出现了“加碘食盐”、“铁强化酱油”、“含氟牙膏”等商品。请回答:
(1)“含氟牙膏”中的氟应理解为 (填序号)。
① 单质 ② 元素
(2)“铁强化酱油”中铁元素的作用是 (填序号)。
① 增加酱油的鲜味 ② 预防缺铁性贫血病 ③ 补充人体需要的铁元素
(3)医学科学家们研究发现,食物中除糖类、脂肪、蛋白质外,还有一类物质与人体健康有着密切关系,它们就是维生素。下列维生素中,可用于防治坏血病的是 。(填序号,下同)
①.维生素A ②.维生素B1 ③.维生素B2 ④.维生素C
(III)世博会中国馆——“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成。①生产玻璃所用的工业设备是 发生的主要反应是
(用化学方程式表示)
②石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是 ;有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种 ,(选填“橡胶”或“纤维”或“塑料”)有机玻璃是由甲基丙烯酸甲酯在一定条件下通过 反应合成的有机高分子材料。
查看答案和解析>>
科目: 来源: 题型:
下列有关化学能与热能的说法正确的是
A.铝热反应属于吸热反应
B.若某反应的反应物的总能量大于生成物的总能量,则该反应为吸热反应
C.H2→H+H的变化需要吸收能量
D.凡经加热而发生的化学反应都是吸热反应
查看答案和解析>>
科目: 来源: 题型:
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。
请回答下列问题:
(1)电池的负极材料为 ,发生的电极反应为 ;
(2)电池正极发生的电极反应为 ;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实![]() 验现象是 ,反应的化学方程式为 ;
验现象是 ,反应的化学方程式为 ;
(4)组装该电池必须在无水、无氧的条件下进行,原因是 。
查看答案和解析>>
科目: 来源: 题型:
钢铁生锈过程发生如下反应
①2Fe+O2+2H2O=2Fe(OH)2; ②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
③2Fe(OH)3=Fe2O3+3H2O。 下列说法正确的是
A.反应①、②中电子转移数目相等
B.反应①中氧化剂是氧气和水
C.与铜质水龙头连接处的钢质水管不易发生腐蚀
D.钢铁在潮湿的空气中不能发生电化学腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com