
科目: 来源: 题型:
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当两装置电路中通过的电子都是1 mol时,下列说法不正确的是
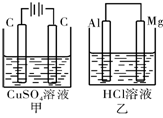
A.溶液的质量变化:甲减小乙增大
B.溶液pH值变化:甲减小乙增大
C.相同条件下产生气体的体积:V甲 = V乙
D.电极反应式:甲中阴极:Cu2+ + 2e- Cu,乙中负极:Mg-2e- Mg2+
查看答案和解析>>
科目: 来源: 题型:
常温下,取浓度相等的NaOH和HCl溶液,以3∶2体积比相混和,所得溶液的PH等于12,则原溶液的浓度为( )
A.0.01mol/L B. 0.017mol/L C. 0.05mol/L D. 0.50mol/L
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D四种短周期元素,原子序数依次增大,A元素原子最外层电子数是次外层的2倍,0.05 mol B元素的离子得到的6.02×1022个电子后被还原为中性原子;0.4g B的氧化物恰好与100mL 0.2mol/L的盐酸完全反应;B元素原子核内质子数与中子数相等。C离子核外电子层数比A元素的离子核外电子层数多1,且形成离子化合物BC,D与A可形成化合物。请填空:
(1)A、B 两种元素的元素符号:B___________ 、C__________。
(2)D与A形成化合物分子式是________,分子空间构型是________。
查看答案和解析>>
科目: 来源: 题型:
右图是生活中常用的锌锰干电池的示意图,下列有关说法中不正确的是
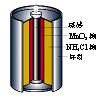
A.电池内部含有电解质
B.锌是负极,碳棒是正极
C.废旧锌锰干电池没有回收价值
D.锌锰干电池属一次电池
查看答案和解析>>
科目: 来源: 题型:阅读理解
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)![]() 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:

①2SO2(g)+O2(g)![]() 2SO3(g)的△H 0(填“>”或“<”);若在恒温、恒
2SO3(g)的△H 0(填“>”或“<”);若在恒温、恒
压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”、“向右”或 “不”);
若在固定容积的密闭容器中发生反应,起始时SO2和O2分别为1mol和0.5mol,达到平衡时SO2的转化率为90%。则从SO3开始进行反应,在相同条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量 ,转化率为
②若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1 K2;若反应进行到状
态D时,![]()
![]() (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
①写出自然界固氮的化学反应方程式: 。
②氨气溶于水得到氨水。在25°C下,将a mol·L-1的氨水与b mol·L-1的盐酸等体积混合,反应后溶液中显中性,则c(NH4+) c(Cl-)(填“>”、“<”或“=”);用含a和b的代数式表示出氨水的电离平衡常数表达式 。
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。在25°C下,向0.1mol·L-1的NaCl溶液中逐滴加入适量的0.1mol·L-1硝酸银溶液,有白色沉淀生成。向反应后的浊液中,继续加入0.1mol·L-1的NaI溶液,看到的现象是 ,产生该现象的原因是(用离子方程式表示) 。
(已知25°C时![]() )
)
查看答案和解析>>
科目: 来源: 题型:
已知:相同温度时,一元弱酸HA的Ka比一元弱酸HB的Ka大。试比较相同温度相同体积的下列两溶液中离子数目的多少。(填“=”、“ >”、“<”、“无法确定”)
(1)物质的量浓度相等的NaA溶液(n1)与NaB溶液(n2),n1 n2
(2)pH相等的NaA溶液(n1)与NaB溶液(n2),n1 n2
(3)c(A—)与c(B—)相等的NaA溶液(n1)与NaB溶液(n2),n1 n2
查看答案和解析>>
科目: 来源: 题型:
下列实验操作中所用的仪器合理的是
A.用25 mL的碱式滴定管量取14.80 mL的KMnO4溶液
B.用100 mL的量筒量取5.2 mL盐酸
C.用托盘天平称取25.20 g氯化钠
D.用250mL的容量瓶配制所需的220mL 0.1mol·L-1的NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com