
科目: 来源: 题型:
白云石的主要成分为CaCO3·MgCO3,还含有少量Fe、Si的化合物。实验室以白云石为原料制备Mg(OH)2及CaCO3。步骤如下:

实验过程中需要的数据见下表:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)溶液A中含有Ca2+、Mg2+、Fe2+、Fe3+,则试剂①可选择_________(填字母,下同);试剂②可选择_________;试剂③可选择_________。
(A)KMnO4(B)Cl2(C)MgO(D)CaO
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是_______,然后通入CO2。通入CO2气体应选择的最佳装置为_______(填字母)。

(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为________________________________。
(4)将制取的Mg(OH)2煅烧得到MgO,然后在还原炉(真空)中,1200℃条件下,用硅铁(铁不参与反应)还原生成镁蒸气。在还原过程中反应温度对生成金属镁的影响如下图:

煅烧Mg(OH)2所需要的仪器除三角架、酒精灯外,还必须选择___________。MgO与硅铁发生的反应达到平衡后,平衡常数表达式为_______________________。由图可知,还原反应的△H ____0(填“>”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
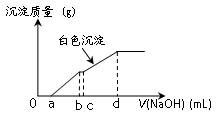
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图,则原混合溶液中MgCl2与FeCl3的物质的量之比为
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
近年来,江苏省酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
⑴有人提出了一种利用氯碱工业产品治理含二氧化硫废气的方法,流程如下: ( I )将含SO2的废气通入电解饱和食盐水所得溶液中,得NaHSO3溶液。(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。(III)将盐酸加入NaHSO3溶液中得SO2气体回收。
① 上述流程中,可循环利用的物质:
② 写出步骤(III)反应的离子方程式:
⑵某实验小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是(填序号) 。
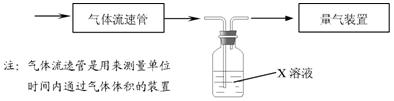
A.碘的淀粉溶液 B.酸性高锰酸钾溶液 C.氢氧化钠溶液 D.氯化钡溶液
(3) 为进一步减少SO2的污染并变废为宝,人们正在探索用CO还原SO2得到单质硫的方法来除去SO2。该方法涉及到的化学反应为:SO2+2CO=2CO2+![]() Sx 、
Sx 、
CO+![]() Sx=COS、2COS+SO2=2CO2+
Sx=COS、2COS+SO2=2CO2+![]() Sx 。其中COS的电子式 。
Sx 。其中COS的电子式 。
(4)若生活污水中含大量的氮化合物,通常用生物膜脱氮工艺进行处理:首先在硝化细菌的作用下将NH4+氧化为NO3-:NH4++2O2=NO3-+2H++H2O,然后加入甲醇,NO3-和甲醇转化为两种无毒气体。请写出加入甲醇后反应的离子方程式 。
查看答案和解析>>
科目: 来源: 题型:
A~L是由6种短周期元素组成的物质,各物质之间有如下转化关系:

已知:
(a) C、E是气体单质,E是一种理想的清洁能源,F是日常生活中的常用金属;
(b) B、J是氧化物,且J是能使澄清石灰水变浑浊的无色无味气体;
(c) 化合物A、D、I、L的焰色反应显黄色;
(d) 白色沉淀K既溶于H溶液,又能溶于D溶液;
(e) 反应①是工业上生产D和C的重要方法。
请回答下列问题:
(1)写出F的化学式 ,D的电子式 。
(2)写出有关反应的化学方程式:
反应① ;
反应② 。
(3)G溶液呈 性(填“酸”、“碱”或“中”),请用离子方程式表示其原因:
。
查看答案和解析>>
科目: 来源: 题型:
在2 L密闭容器中,发生3A(g)+B(g)![]() 2C(g)的反应,若最初加入A和B都是4 mol,A的平均反应速率为0.12 mol·L-1·s-1,则10 s后容器中B的物质的量浓度是( )
2C(g)的反应,若最初加入A和B都是4 mol,A的平均反应速率为0.12 mol·L-1·s-1,则10 s后容器中B的物质的量浓度是( )
A.1.4 mol·L-1 B.1.6 mol·L-1
C.1.8 mol·L-1 D.3.2 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
回答下列有关问题:
(1)硫化铵水解的离子方程式为:S2-+NH4++H2O![]() HS-+ NH3·H2O,
HS-+ NH3·H2O,
如何判断溶液的酸碱性: 。
(2)污水中含有Hg2+,用难溶的FeS作为沉淀剂可使Hg2+转化为HgS而除去,该反应能进行的依据是: 。有人认为加入FeS作为沉淀剂还可以起到净化水的作用,请你运用所学知识解释:
。
(3)用离子方程式解释泡沫灭火器(将硫酸铝与碳酸氢钠溶液混和)灭火原理:
。
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是:
A.蛋白质、纤维素、蔗糖、PVC、淀粉都是高分子化合物
B.氢键在形成蛋白质二级结构和DNA双螺旋结构中起关键作用
C.使用太阳能热水器、沼气利用、玉米制乙醇都涉及到生物质能的利用
D.石油、煤、天然气、可燃冰、植物油都属于化石燃料
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W四种短周期元素在周期表中相对位置如表所示,Y、Z质子数之和为21,下列说法中不正确的是 ( )
A.X、Y、Z、W均为非金属元素
B.Y、Z形成的化合物为离子晶体
C.Z的阳离子与Y的阴离子电子层结构相同
D.X、Y、W的氢化物中,Y的氢化物沸点最高
查看答案和解析>>
科目: 来源: 题型:
下列各组离子在给定条件的溶液中可能大量共存的是 ( )
A.加入铝粉有大量氢气产生的溶液中:Mg2+、K+、NO3-、C1-
B.PH = 0的无色溶液中:Na+、K+、MnO4-、NO3-
C.在0.1mol/L的醋酸溶液中:Fe2+、Na+、ClO-、Ca2+
D.在c(OH-)= 1×10-13的溶液中:NH4+、Ca2+、C1-、K+
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是
A.a原子的最外层电子数比B原子的最外层电子数少
B.常温时,a能从水中置换出氢,而b不能
C 1mol a从酸中置换H+生成的![]() 比l mol b从酸中置换
比l mol b从酸中置换![]() 生成的
生成的![]() 多
多
D.a原子电子层数比b原子的电子层数多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com