
科目: 来源: 题型:
碳正离子[例如,CH3+,CH5+,(CH3)3C+等]是有机反应中重要的中间体。欧拉(G.Olah)因在此领域研究中的卓越成就而获荣获1994年诺贝尔化学奖。碳正离子CH5+可以通过CH4在“超强酸”中再获得一个H+而得到;而CH5+失去H2,可以得到CH3+。
(1)CH3+是反应性很强的正离子,是缺电子的,其电子式是
(2)CH3+中4个原子时共平面,三个键角相等。键角应是___________
(3)(CH3)2CH+在NaOH的水溶液中反应将得到电中性的有机分子,其结构简式是 。
(4) (CH3)3C+去掉H+后将生成电中性的有机分子,其结构简式是 。
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.正四面体型的分子结构中键角均为109°28′
B.在晶体中只要有阳离子就一定有阴离子
C.发生化学反应时失去电子越多的金属原子,还原能力越强
D.两种微粒的质子数和电子数均相等,则它们不可能是带异性电荷的离子
查看答案和解析>>
科目: 来源: 题型:
下列实验过程中产生的现象与对应的图形符合的是
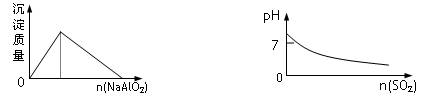
A.盐酸中加入NaAlO2溶液 B.SO2气体通入溴水中
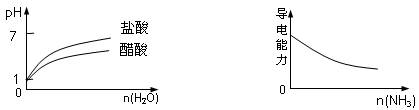
C.pH=1的醋酸与盐酸分别加水稀释 D.氨气通入醋酸溶液中
查看答案和解析>>
科目: 来源: 题型:
Co(Ⅲ)的八面体配合物CoClm· nNH3 ,若1mol配合物与AgNO3作用生成1molAgCl沉淀,则m、n的值是( )
A.m=1 n=5 B.m=3 n=4 C.m=5 n=1 D.m=4 n=5
查看答案和解析>>
科目: 来源: 题型:
某实验小组设计用50 mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在下图装置中进行中和反应。在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
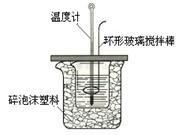
(1)本实验中用稍过量的NaOH的原因教材中说是为保证盐酸完全被中和。试问:盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热数值 (填偏高、偏低或不变);
(2)该实验小组做了三次实验,每次取溶液各50mL,并记录如下原始数据。
| 实验序号 | 起始温度t1/℃ | 终止温度(t2)℃ | 温差(t2-t1)℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
已知盐酸、NaOH溶液密度近似为1.00g/cm3中和后混和液的比热容 C=4.18J(g.·℃)则该反应的中和热为△H=___________________________________;
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热的数值会 (填偏高、偏低或不变),其原因是 ;
(4)影响中和热测定结果的关键因素在于:
为减小实验误差,可采取的措有: 。
查看答案和解析>>
科目: 来源: 题型:
Co(NH3)5BrSO4可形成两种钴的配合物 ,已知两种配合物的分子式分别为[Co(NH3)5Br] SO4 和[Co (SO4) (NH3)5] Br, 在第一种配合物的溶液中加BaCl2 溶液时, 产生 现象 ;如果在第二种配合物的溶液中加入BaCl2溶液时,产生 现象,若加入 AgNO3溶液时,产生 现象。
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是( )
A.NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构
B.P4和CH4都是正四面体分子且键角都为109o28ˊ
C.NaCl晶体中与每个Na+距离相等且最近Na+共有12个
D.CsCl晶体中与每个Cs+距离相等且最近Cl-共有6个
查看答案和解析>>
科目: 来源: 题型:
下列说法或表示方法不正确的是
A.燃料的燃烧反应都是放热反应
B.绿色植物进行光合作用时,能把光能转化为化学能
C.分子的热稳定性主要取决于分子内化学键的键能大小,与分子间作用力无关
D.已知:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4 kJ·mol-1,则说明相同条件下,在密闭容器中,1 mol N2和3 mol H2混合充分反应后放热92.4 kJ
2NH3(g) △H=-92.4 kJ·mol-1,则说明相同条件下,在密闭容器中,1 mol N2和3 mol H2混合充分反应后放热92.4 kJ
查看答案和解析>>
科目: 来源: 题型:
用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,为了降低化学反应的反应速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水 B.加热 C.NaCl固体 D.浓盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com