
科目: 来源: 题型:
由1~18号元素组成的化合物X是某抗酸药的有效成分。某同学欲探究X的组成。
查阅资料:①由1~18号元素组成的抗酸药的有效成分可能是碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、磷酸铝、碱式碳酸镁铝。
②Al3+在pH=5.0时沉淀完全;Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全。
实验过程:
Ⅰ.向化合物X粉末中加入过量盐酸,产生气体A,得到无色溶液。
Ⅱ.用铂丝蘸取少量Ⅰ中所得的溶液,在火焰上灼烧,无黄色火焰。
Ⅲ.向Ⅰ中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤。
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解。
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C。
⑴Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是___________。
⑵由Ⅰ、Ⅱ判断X一定不含有的元素是磷、___________(填元素名称)。
⑶Ⅲ中生成B的离子方程式是___________。
⑷Ⅳ中B溶解的离子方程式是___________。
⑸沉淀C的化学式是___________。
⑹若上述n(A):n(B):n(C)=1:1:3,则X的化学式是___________。
查看答案和解析>>
科目: 来源: 题型:
白色的Fe(OH)2沉淀在空气中极易被氧化。利用如右图装置可以制得白色的Fe(OH)2沉淀,并能在较长时间内保持白色。实验中可选用的试剂有:NaOH溶液、铁屑、稀H2SO4。

⑴Fe(OH)2在空气中被氧化的化学方程式是__________________,实验现象是__________________。
⑵在试管Ⅰ里加入的试剂是__________;在试管Ⅱ里加入的试剂是__________。
⑶在试管Ⅰ和Ⅱ中加入试剂后的实验操作依次是___________(选填序号)。
①检验A口排出气体的纯度
②夹紧止水夹
③打开止水夹
⑷这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是________________________。
查看答案和解析>>
科目: 来源: 题型:
向4.2 g NaHCO3粉末中加入一定体积1 mol/L的盐酸,恰好完全反应。试计算:
⑴加入盐酸的体积;
⑵反应生成气体的体积(标准状况);
⑶假设反应前后溶液体积不变,所得溶液中Na+的物质的量浓度。
查看答案和解析>>
科目: 来源: 题型:
铝土矿的主要成分是Al2O3,含有杂质SiO2、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如下工艺流程:

请回答下列问题:
⑴图中涉及分离溶液与沉淀的实验方法是__________(填操作名称)。
⑵沉淀B的成分是___________(填化学式,下同);
沉淀C的成分是___________;
溶液D中大量存在的阴离子是___________。
⑶沉淀F转化为物质M的化学方程式为___________;
由物质M制取铝的化学方程式为___________;
溶液D中通入过量CO2生成沉淀F的离子方程式为__________。
查看答案和解析>>
科目: 来源: 题型:
Ⅰ下面是几种实验中常用的仪器:


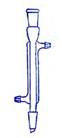
![]()
A B C D
写出序号所代表的仪器的名称:
A___________;B___________;C___________;D___________
Ⅱ实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题:
⑴配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和___________。
⑵用托盘天平称取氯化钠固体,其质量为__________ g。
⑶下列主要操作步骤的正确顺序是___________(填序号)。
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
⑷如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______(填“偏高”或“偏低”或“无影响”,下同);若定容时俯视容量瓶刻度线,会造成所配溶液的物质的量浓度_________。
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述中,正确的是
A.0.1 mol Na变成Na2O2时,失去0.2NA个电子
B.NA个N2与NA个H2的质量比等于14:1
C.常温常压下,11.2 L CO2中所含的分子数为0.5NA
D.4 g NaOH溶解于500 mL水中,所得溶液的物质的量浓度为0.2 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
某溶液中含有较大量的Mg2+、Ag+、Ba2+ 3种阳离子,欲将3种离子逐一沉淀出来,下列加入试剂的顺序中,正确的是
①NaOH溶液、NaCl溶液、Na2SO4溶液
②NaOH溶液、Na2SO4溶液、NaCl溶液
③NaCl溶液、Na2SO4溶液、NaOH溶液
④NaCl溶液、NaOH溶液、Na2SO4溶液
A.①② B.③④ C.①③ D.②④
查看答案和解析>>
科目: 来源: 题型:
下列事实能用金属活动性顺序表解释的是
A.使用铝制水壶烧水
B.用铁丝而不用铜丝做焰色反应的实验
C![]() .工业上常用热还原法冶炼铁,用电解法冶炼钠
.工业上常用热还原法冶炼铁,用电解法冶炼钠
D.铝既能与强酸溶液反应,也能与强碱溶液反应
查看答案和解析>>
科目: 来源: 题型:
下列关于金属钠的叙述中,正确的是
A.为防止钠与水反应时燃烧,可将该反应置于试管中进行,以减少与氧气的接触
B.钠着火时应用干燥的沙土灭火
C.钠在空气中受热时,熔化为银白色的小球,产生黄色的火焰,生成白色粉末
D.钠在空气中长期放置,最终主要生成物为过氧化钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com