
科目: 来源: 题型:
下列离子方程式,一定正确的是 ( )
A.铝铵矾[NH4Al(SO4)2·12H2O]溶液中加入过量Ba(OH)2溶液:
Al3++2SO2-4+2Ba2++4OH-=AlO-2+2BaSO4↓+2H2O
B.H2O2溶液中滴加酸性KMnO4溶液:2MnO-4+5H2O2+6H+=2Mn2++5O2↑+8H2O
C.铁屑溶于过量稀硝酸:3Fe+8H++2NO-3=3Fe2++2NO↑+4H2O
D.少量NaHSO4溶液与足量Ba(OH)2溶液反应:2H++SO2-4+Ba2++2OH-=BaSO4↓+2H2O
查看答案和解析>>
科目: 来源: 题型:
下列液体均处于25℃,有关叙述正确的是 ( )
A.某物质的溶液pH <7,则该物质一定是酸或强酸弱碱盐
B.AgCl在相同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
C.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)> c(CH3COO一)
D.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
查看答案和解析>>
科目: 来源: 题型:
若NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.0.2 mol过氧化氢完全分解转移的电子数目为0.4 NA
B.12.8g Cu与足量HNO3反应生成NO和NO2,转移电子数目为0.2 NA'
C.1 mol C3OH62分子中含有共价键的数目为91 NA
D.1 mol SiO2晶体中含有NASiO2个分子
查看答案和解析>>
科目: 来源: 题型:
化学已渗透到人类生活的各个方面。下列说法不正确的是 ( )
A.人造纤维、合成纤维和光导纤维都是有机高分子化合物
B.可以用Si3N4、Al2O3制作高温结构陶瓷制品
C.地球上CH4、CO2等气体含量上升容易导致温室效应加剧,进而引发灾难性气候
D.禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染
查看答案和解析>>
科目: 来源: 题型:
发展低碳经济、减少能源消耗、走可持续的发展之路,这对中国经济发展既是机遇也是挑战,下列说法不正确的是 ( )
A.积极开发风能发电和水力发电。
B.尽量用纯液态有机物代替水作溶剂。
C.提高原子利用率,发展绿色化学
D.积极开发半导体节能灯具
查看答案和解析>>
科目: 来源: 题型:
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为 。利用反应6NO2+ 8NH3![]() 7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知: 2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡
 状态的是 。
状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K= 。
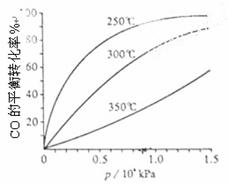
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如上图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如上图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
查看答案和解析>>
科目: 来源: 题型:
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,As2S3和SnCl2的物质的量之比为 。
(2)上述反应中的氧化剂是 ,反应产生的气体可用 吸收。
(3) As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成2mol H3AsO4,则反应中转移电子的物质的量为 。若将该反应设计成一原电池,则NO2应该在 (填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,所产生的CO2的量 (选填编号)。
a.小于0.5 mol b.等于0.5 mol c.大于0.5mol d.无法确定
查看答案和解析>>
科目: 来源: 题型:阅读理解
I、磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子结构示意图是____________。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2===6CaSiO3+P4O10 10C+P4O10===P4+10CO
每生成1 mol P4时,就有________mol电子发生转移。
(3)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I- 2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入a mol·L-1 I2溶液V1 mL,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗b mol·L-1 Na2S2O3溶液V2 mL。该溶液中维生素C的物质的量是__________mol。
(4)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3-+5SO32-+2H+===I2+5SO42-+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
| 0.01mol·L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol·L-1Na2SO3溶液的体积/mL | H2O的体积/mL | 实验温度 /℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
该实验的目的是_____________________;表中V2=___________mL
II、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(5)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是______________。
(6)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
□Ce3++□H2O2+□H2O === □Ce(OH)4↓+□_______
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏伽德罗常数的值。下列叙述正确的是
A.1mol甲醇中含有C—H键的数目为4NA
B.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA
C.标准状况下,2.24L已烷含有分子的数目为0.1NA
D.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA
查看答案和解析>>
科目: 来源: 题型:
NA为阿伏伽德罗常数,下列叙述错误的是
A.18gH2O中含的质子数为10NA
B.12g 金刚石含有的共价键数为4NA
C.46gNO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com