
科目: 来源: 题型:
实现Al3++3AlO2-+6H2O=4Al(OH)3↓,正确的做法是( )
A.向铝盐溶液中不断加入纯碱溶液 B.向铝盐溶液中不断加入小苏打溶液
C.向烧碱溶液中不断滴入铝盐溶液 D.向铝盐溶液中不断滴入烧碱溶液
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是 ( )
A.发生化学反应时失去电子越多的金属原子, 还原能力越强
B.金属阳离子被还原后,一定得到该元素的单质
C.核外电子总数相同的原子,一定是同种元素的原子
D.能与酸反应的氧化物,一定是碱性氧化物
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W有如右图所示的转化关系,则X、Y可能是 ( )
①C、CO ②AlCl3、Al(OH)3
③Fe、Fe(NO3)2 ④Na2CO3、NaHCO3
A.①②③④ B.①②
C.③④ D.①③

查看答案和解析>>
科目: 来源: 题型:
向含有FeCl2、FeCl3、AlCl3、NH4Cl的混合溶液中先加入过量Na2O2固体,微热搅拌后再加入过量盐酸,溶液中阳离子数目变化最小的是 ( )
A.Fe2+ B.Fe3+ C.Al3+ D.NH4+
查看答案和解析>>
科目: 来源: 题型:
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平,下图表示了三种金属被人类开发利用的大致年代,之所以有先后,主要取决于 ( )
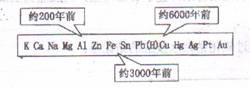
A.金属的导电性强弱 B.金属在地壳中的含量多少
C.金属的化合价高低 D.金属的活动性大小
查看答案和解析>>
科目: 来源: 题型:
纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。
 单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
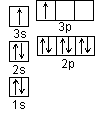
(1)某同学根据上述信息,推断B的核外电子排布如右图所示,
该同学所画的电子排布图违背了 。
(2)根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为 。
 (3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 ,并阐述理由 。
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确 ,并阐述理由 。
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物, 其晶胞如图所示,该物质在低温时是一种超导体。写出基态钾原子的电子排布式 ,该物质的K原子和C60分子的个数比为 。
(5)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为 。
查看答案和解析>>
科目: 来源: 题型:
一定量的氢气在氯气中燃烧,所得混合物用100mL 4.00mol/L的NaOH溶液(密度为1.20g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0. 0800mol。(以下计算要有计算过程)
(1)求原NaOH溶液的质量分数为多少?
(2)求所得溶液中Cl-的物质的量。
(3)所用氯气和参加反应的氢气的物质的量之比为多少?
查看答案和解析>>
科目: 来源: 题型:
2 g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075 mol/L KMnO4溶液处理,反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的 KMnO4恰好与350 mL 0.1 mol/L (NH4)2Fe(SO4)2 溶液完全反应,反应的离子方程式:MnO4-+5Fe2++8H+=Mn2++5 Fe3+ +4H2O
(1) KMnO4溶液与混合物反应,消耗KMnO4的物质的量为 mol。
(2)欲配制500mL 0.1mol/L NH4+ 溶液,需称取 (NH4)2Fe(SO4)2·6H2O (M=392g/mol)
的质量为 g。
(3)混合物中 Cu2S的质量分数为 。
查看答案和解析>>
科目: 来源: 题型:
为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。
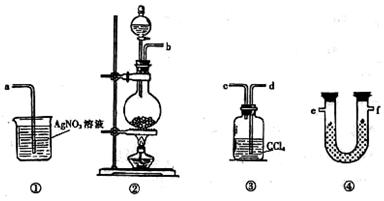
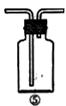
⑴请根据甲同学的意图,连接相应的装置,接口顺序:
b接________,__________接 _________,_________接a。
⑵U形管中所盛试剂的化学式为_____________________________ 。
⑶装置③中CCl4的作用是___________________________________。
⑷乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加装置⑤。你认为装置⑤应加在_____________之间(填装置序号)。瓶中可以放入______________________________________。
⑸丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成__________________________,如果观察到_______________________________的现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目: 来源: 题型:
下图每一方框中的字母代表一种反应物或生成物,它们都是中学化学中常见的物质。产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,L是水,D是淡黄色固体,E为单质。
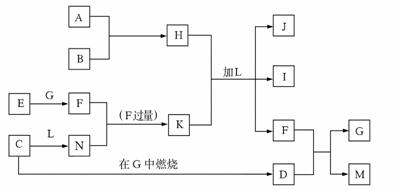
试填写下列空白:
(1)写出F的化学式: _______________。
(2)写出M发生水解的化学反应方程式__________________。 (3)反应C+G→D的化学方程式是_______________。 (4)写出H 、K加L生成J、I、F反应的离子方程式_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com