
科目: 来源: 题型:
a | |||||||||||||||||
b | c | d | |||||||||||||||
e | f | g | |||||||||||||||
h |
试回答下列问题:
(1)元素h的二价阳离子的基态电子排布式为 。
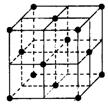
(2)在1185 K时,元素h可形成如图所示基本结构单元的晶体,
则其中h原子的配位数是 。
(3)c、d、e、f元素的第一电离能(I1)由小到大的顺序
为 。(用相应元素符号表示)
(4)表中所列的元素之间可以形成多种化合物,其中邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,理由是 。邻甲基苯甲醛分子中碳原子轨道的杂化类型为 。1 mol 苯甲醛分子中σ键为 mol。
(5)一种由表中元素形成的离子与单质d3互为等电子体,其化学式为 。
查看答案和解析>>
科目: 来源: 题型:
某硝酸厂附近的空气主要污染物为氮的氧化物。为了保护环境和综合利用,可采用氨-碱两级吸收法。此法兼有碱吸收和氨吸收两法的优点,其吸收工艺流程如下:
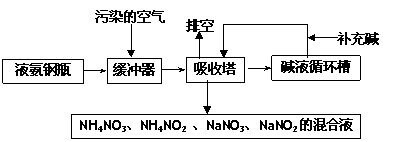 |
(1)排空物质的主要成分为____________________________。
(2)进入吸收塔以前加一个缓冲器的目的是________________________________。
(3)从吸收塔排出的混合液用途之一为________________ 。
空气的主要污染物为硫的氧化物和氮的氧化物。研究人员设计了同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如下:
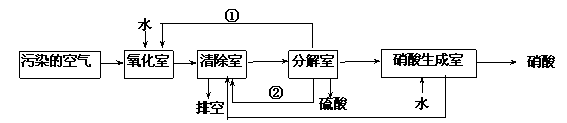
各室中发生的反应如下:
a.氧化室:NO2(g) + SO2(g) + H2O (l)=H2SO4 (l)+ NO(g)△H=a kJ·mol-1
b.清除室:NO (g)+ NO2 (g)= N2O3(g) △H= b kJ·mol-1
N2O3 (g)+ 2H2SO4(l) = 2NOHSO4 (s)+ H2O(l) △H=c kJ·mol-1
c.分解室:4NOHSO4 (s)+ O2 (g)+ 2H2O (l)= 4H2SO4 (l)+ 4NO2(g) △H= dkJ·mol-1
回答下列问题:
(4)①和②分别为(写化学式)______________、_____________。
(5)写出SO2、 O2 和 H2O反应生成H2SO4的热化学方程式:
____________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。已知: §SO2(g) +1/2O2(g)![]() SO3(g) △H=-98 kJ·mol-1。
SO3(g) △H=-98 kJ·mol-1。
(1)某温度下该反应的平衡常数K=10/3,若在此温度下,向100 L的恒容密闭容器中,充入3.0 mol SO2(g)、16.0 mol O2(g)和3.0 mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”)。
(2)一定温度下,向一带活塞的体积为2 L的密闭容器中充入2.0 mol SO2和1.0 mol O2,达到平衡后体积变为1.6 L,则SO2的平衡转化率为 。
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是 (填字母)。
A.保持温度和容器体积不变,充入1.0 mol O2
B.保持温度和容器内压强不变,充入1.0 mol SO3
C.降低温度
D.移动活塞压缩气体
(4)若以右图所示装置,用电化学原理生产硫酸,写出通入O2电极的电极反应式为 。
(5)为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量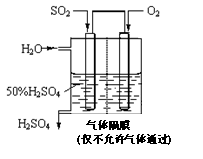 比为____________。
比为____________。
查看答案和解析>>
科目: 来源: 题型:
重晶石矿石主要含有BaSO4,还含有少量的SiO2、Al2O3、Fe2O3、MnO2、
FeS2、Na2O、K2O等杂质。以下是某工业制备硫酸钡以及分离某些金属的流程图。
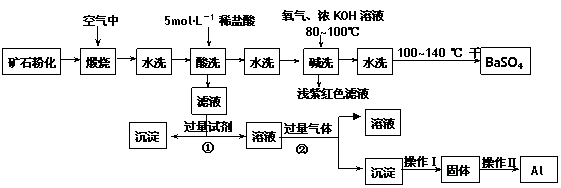
(1)煅烧过程中产生的污染性气体主要是 。
(2)确定第一次水洗液中有K+存在的实验现象是 。
(3)写出碱洗时的氧化还原反应方程式 。
(4)①反应生成沉淀的化学式 ,②反应的离子方程式为 。
(5)操作Ⅰ为 ,操作Ⅱ为 。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E都是中学化学中常见物质,它们均含有同一种短周期元素,在一定条件下可发生如右图所示的转化,其中A是单质,B常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物。下列判断中不合理的是
A.A不可能是金属 B.由C生成D肯定发生了电子转移
C.A生成C肯定属于离子反应 D.B和E可能会发生反应生成一种盐
查看答案和解析>>
科目: 来源: 题型:
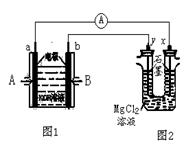
下图中,图1为甲烷和O2构成的燃料电池,图2为电解MgCl2溶液装置。用该装置进行实验,反应开始后,观察到x电极附近出现白色沉淀。下列说法正确的是
A.A处通入的气体为CH4,B处通入的气体为O2
B.电池内部K+向b极移动,老虎OH-向a极移动
C.图1装置中发生的总反应为:
CH4+2O2===CO2+3H2O
D.图1、图2中电解质溶液的pH均增大
查看答案和解析>>
科目: 来源: 题型:
下列溶液中微粒的物质的量浓度关系正确的是
A.0.1 mol·L-1的NH4Cl溶液与0.05 mol·L-1的NaOH溶液等体积混合后的溶液:
c(Cl-) > c(Na+) > c(NH4+) > c(OH-) > c(H+)
B.等物质的量的NaClO、NaHCO3混合溶液中:
c(HClO) + c(ClO-) = c(HCO3-) + c(H2CO3) + c(CO32-)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:
c(M+) = c(A-)>c(OH-) = c(H+)
D.某二元弱酸的酸式盐NaHA溶液:c(OH-) + c(H2A) = c(H+) + 2c(A2-)
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式中正确的是
A.硫酸亚铁溶液在空气中氧化:Fe2++3O2+6H2O=4Fe(OH)3↓
B.向苯酚溶液中滴入少量Na2CO3溶液:

C.向Na2SO3、NaI的混合溶液中滴加少量氯水:2I -+Cl2==2Cl-+I2
D.1mol·L-1的NaAl溶液和2.5 mol·L-1的HCl溶液等体积混合:
2AlO2-+5H+ =Al(OH)3↓+Al3++H2O
查看答案和解析>>
科目: 来源: 题型:
科学家研制出多种新型杀虫剂代替DDT,化合物A是其中的一种。下列关于A的说法正确的是
A.A的分子式为C15H22O3
B.与FeCl3溶液发生反应后溶液显紫色
C.分子中有3个手性碳原子
|
查看答案和解析>>
科目: 来源: 题型:
下列化学实验事实及其解释都正确的是
A.氯气可以使湿润的有色布条褪色,是因为氯气具有漂白性
B.SO2溶于水,其水溶液能导电,说明SO2是电解质
C.用饱和Na2CO3溶液可将BaSO4转化为BaCO3,说明Ksp(BaSO4)>Ksp(BaCO3)
D.某溶液用盐酸酸化无明显现象,再滴加氯化钡溶液有白色沉淀产生,说明溶液中有SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com