
科目: 来源: 题型:
在一个容积不变的反应容器中,可以通过调节温度使下列反应:A(g)+2B(g)![]() 2C(g) 达到平衡时保持容器内气体的总物质的量为15 mol。现向反应容器中加6.5 mol A、X mol B、4 mol C。
2C(g) 达到平衡时保持容器内气体的总物质的量为15 mol。现向反应容器中加6.5 mol A、X mol B、4 mol C。
(1)若X=5.5时需要降低体系温度才能使反应达平衡时符合题设条件,则正反应为_________反应。(填“吸热”或“放热”)
(2)欲使该反应起始时维持逆向移动,则X的取值范围_________________________。
查看答案和解析>>
科目: 来源: 题型:
自然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,压强增大约25000~30000 kPa。在地壳内SiO2和HF存在以下平衡:SiO2(s) +4HF(g)![]() SiF4(g)+ 2H2O(g) △H =-148.9 kJ·mo1-1
SiF4(g)+ 2H2O(g) △H =-148.9 kJ·mo1-1
根据题意完成下列填空:
(1)在地壳深处容易有 气体逸出,在地壳浅处容易有 沉积。
(2)如果上述反应的平衡常数K值变大,该反应 (选填编号)。(3分)
a.一定向正反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为 。(3分)
查看答案和解析>>
科目: 来源: 题型:
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数的测定。
实验步骤:将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)![]() 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
(1)可以判断该分解反应已经达到化学平衡的是___________。
A.![]() B.密闭容器中总压强不变
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
(2)根据表中数据,计算25.0℃时的分解平衡常数:__________________________。
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量______(填“增加”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应
SO2(g)+NO2(g)![]() SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。
(1)点a-c段,速率变化的主要原因是 ,点c后速率变化的主要原因是 。
(2)c点是否已经达到平衡状态 (填“是”、“否”或“不一定”)
(3)反应物浓度:a点 b点(填“<”、“=”或“>”)
(4)反应物的总能量 生成物的总能量(填“<”、“=”或“>”)
(5)△t1=△t2时,SO2物质的量的变化量:a~b段 b~c段(填“<”、“=”或“>”)

查看答案和解析>>
科目: 来源: 题型:
写出下列反应的热化学方程式:
(1)已知0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量,写出能表示该反应燃烧热的热化学方程式
(2)NA表示阿伏加德罗常数,在CH4(g)完全燃烧生成CO2和液态水的反应中,每有4NA个电子转移时,放出445kJ的热量。____________________________________________
(3)已知拆开1molN≡N键,1molH-H键,1molN-H键分别需要的能量是a kJ、b kJ、
c kJ,则N2与H2反应生成NH3的热化学方程式为__________________________________
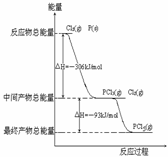
(4)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
①P和Cl2反应生成PCl3的热化学方程式
②PCl5分解成PCl3和Cl2的热化学方程式_______________________
查看答案和解析>>
科目: 来源: 题型:
下列实验事实所引出的相应结论正确的是( )
| 选项 | 实验事实 | 结论 |
| A | Na2S2O3溶液与稀H2SO4溶液混合时,其他条件相同,Na2S2O3溶液浓度越大,析出硫沉淀所需时间越短 | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参加化学反应 |
| C | 将NH4Cl晶体与Ba(OH)2.8H2O晶体混合后研磨,烧杯壁温度降低 | 该反应为吸热反应 |
| D | 在容积可变的密闭容器中发生反应 H2(g)+ I2(g) 把容积缩小一倍 | 正反应速率加快,逆反应速率不变 |
查看答案和解析>>
科目: 来源: 题型:
根据碘与氢气反应的热化学方程式
①I2(g)+ H2(g) ![]() 2HI(g)△H= -9.48 kJ/mol
2HI(g)△H= -9.48 kJ/mol
②I2(s)+ H2(g)![]() 2HI(g) △H= +26.48 kJ/mol
2HI(g) △H= +26.48 kJ/mol
下列判断正确的是( )
A.254g I2(g)中通入2gH2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应①的产物比反应②的产物稳定
D.反应②的反应物总能量比反应①的反应物总能量低
查看答案和解析>>
科目: 来源: 题型:
已知一定温度和压强下,N2(g)和H2(g)反应生成2mol NH3(g),放出92.4kJ热量。在同温同压下向密闭容器中通入1mol N2和3mol H2,达平衡时放出热量为Q1kJ;向另一体积相同的容器中通入0.5mol N2和1.5mol H2,相同温度下达到平衡时放出热量为Q2kJ。则下列叙述正确的是( )
A.2Q2>Q1=92.4kJ B.2Q2=Q1=92.4kJ
C.2Q2<Q1<92.4kJ D.2Q2=Q1<92.4kJ
查看答案和解析>>
科目: 来源: 题型:
在一定温度下,向一个容积可变的恒压容器中,通入3 mol SO2和2 mol O2及固体催化剂,使之反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4 mol SO2、3 mol O2、2 mol SO3(g),下列说法正确的是( )
2SO3(g) ΔH=-196.6 kJ·mol-1,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4 mol SO2、3 mol O2、2 mol SO3(g),下列说法正确的是( )
A.第一次实验平衡时反应放出的热量为98.3kJ
B.第一次实验平衡时SO2的转化率比第二次实验平衡时SO2的转化率大
C.第二次实验达平衡时SO3的体积分数大于2/9
D.两次实验平衡时,SO3的浓度相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com