
科目: 来源: 题型:
分析右边的能量变化示意图,下列热化学方程式正确的是
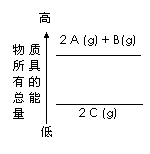 |
A.2A(g)+ B(g)=2C(g) △H=a(a>0)
B.2A(g)+ B(g)=2C(g) △H=a(a<0)
C.2A + B = 2 C △H=a(a<0)
D.2C =2A + B △H=a(a>0)
查看答案和解析>>
科目: 来源: 题型:
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3-)变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①分别用0.1 mol/L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
②与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快 B.H2SO4最快 C.CH3COOH最快 D.一样快
(3)某温度下,纯水中c(H+)=2×10-7 mol/L,则此时0.02mol/LBa(OH)2溶液的pH =
(4)有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
查看答案和解析>>
科目: 来源: 题型:
铅蓄电池是典型的可充型电池,它的正负极板是惰性材料,
电池总反应式为:
Pb+PbO2+4H++2SO42-2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是___________________________;电解质溶液中H2SO4的浓度将_______ (填“变大”、“ 变小”或“不变”);当外电路通过1 mol电子时,理论上负极板的质量增加_______ g。
(2)在完全放电耗尽PbO2和Pb时,若按图连接,电解一段时间后,则在A电极上生成____________、B电极上生成______________,此时铅蓄电池的正负极的极性将_______________________。

查看答案和解析>>
科目: 来源: 题型:
下图中每一方框中的字母代表一种反应物或生成物(部分产物未列出):
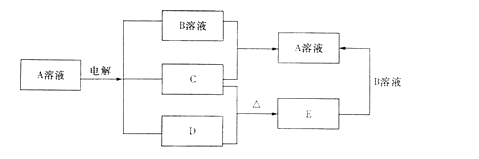
已知C是紫红色金属固体,B的浓溶液和稀溶液都是有强氧化性。
(1)A的化学式是 ,E化学式是 ;
(2)电解反应的化学(或离子)方程式是 ;
(3)对200ml 1mol/L的A溶液进行电解,当有0.02mol电子发生转移时,溶液的![]() 为
为
(假设溶液体积不变)。
查看答案和解析>>
科目: 来源: 题型:
下列各溶液中,微粒的物质的量浓度关系正确的是
A.10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合:
c(Cl-)>c(Na+)>c(OH-)>c(H+)
B.0.1 mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:
c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl)
查看答案和解析>>
科目: 来源: 题型:
电解质溶液有许多奇妙之处,你只有深入的去思考,才能体会到它的乐趣。下列关于电解质溶液的叙述中正确的是
A.Na2CO3、NaHCO3两种盐溶液中,离子种类相同
B.常温下,1 mol·L-1的CH3COOH溶液与1 mol·L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C.物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者大于后者
D.常温下,某溶液中由水电离出的c(H+)=10-5 mol·L-1,则此溶液可能是盐酸
查看答案和解析>>
科目: 来源: 题型:
下列叙述错误的是
A.把a L 0.1 mol/L 的CH3COOH溶液与b L 0.1 mol/L的 KOH溶液混合,所得溶液中一定存在:c (K+)+ c (H+) = c (CH3COO-) + c (OH-)
B.把0.1 mol/L 的NaHCO3溶液与0.3 mol/L 的Ba(OH)2溶液等体积混合,所得溶液中一定存在:c (OH-) >c (Ba2+)>c (Na+)> c (H+)
C.向1 mol/L 的CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高
D.常温下,在pH=3的CH3COOH溶液和pH=11的NaOH溶液中,水的电离程度相同
查看答案和解析>>
科目: 来源: 题型:
已知反应:2SO2(g)+O2(g) ![]() 2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g);ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是

A.由图甲知,A点SO2的平衡浓度为0.4 mol·L-1
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2:1:2
C.达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目: 来源: 题型:
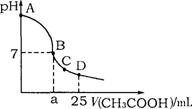
在25mL 0.1mol·L-1NaOH溶液中逐滴加入0. 2mol·L-1CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是
A.在A、B间任一点(不含A、B点),
溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.在D点,c(CH3COO-)+c(CH3COOH)=c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com