
科目: 来源: 题型:
下列电离方程式书写不正确的是( )
A、2H2O ![]() H3O++OH- B、H2S
H3O++OH- B、H2S ![]() H++HS-
H++HS-
C、NaHS ![]() Na++HS- D.HCO3-+H2O
Na++HS- D.HCO3-+H2O ![]() H3O++CO32-
H3O++CO32-
查看答案和解析>>
科目: 来源: 题型:
金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(s,mol·L-1)见右图。
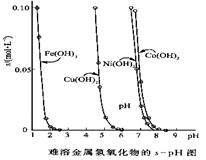 (1)pH=3时溶液中铜元素的主要存在形式是:________(化学式)
(1)pH=3时溶液中铜元素的主要存在形式是:________(化学式)
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,___ (能、不能)通过调节溶液pH的方法来除去,理由是_________。
(4)已知一些难溶物的溶度积常数如下表。
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
某工业废水中含有Cu2+、Pb2+、Hg2+,最适宜向此工业废水中加入过量的_______除去它们。
A.NaOH B.FeS C.Na2S
查看答案和解析>>
科目: 来源: 题型:
处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S(g)。发生反应为:2CO(g)+SO2(g) ![]() S(g)+2CO2(g)
S(g)+2CO2(g)
(1)已知:CO(g)+![]() O2(g)=CO2(g) △H=-283.0kJ·mol—1
O2(g)=CO2(g) △H=-283.0kJ·mol—1
S(g)+O2(g)=SO2(g) △H= - 296.0 kJ·mol—1
试写出利用上述方法处理烟道气的热化学方程式
(2)在容积为2L的密闭容器中,充入4molCO和2molSO2,在一定条件下发生反应2CO(g)+SO2(g) S(g)+2CO2(g),CO2的物质的量分数随时间的变化如图所示,则:
①0-2min内的平均反应速率v(CO)= 。
②该温度下,上述反应的平衡常数K= (填数值)。
③2min后改变下列条件能使上述反应的反应速率增大,且平衡向正 向移动的是
a.选用更高效的催化剂 b.升高温度 c.及时分离出二氧化碳 d.增加SO2的浓度

查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的离子不含电子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
(1)C元素在元素周期表中的位置是
(2)C和E两种元素相比较,非金属性较强的是(填元素名称) ,可以验证该结论的是(填写编号) ;
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
(3)A、C、E间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为 ;
(4)F含有的化学键类型是 ,其水溶液呈酸性,请用相关的离子方程式解释其原因
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为
查看答案和解析>>
科目: 来源: 题型:
利用右图装置收集以下几种气体(图中烧瓶位置不得移动)
H2、Cl2、NO2、HCl、NH3、NO
(1)若烧瓶是干燥的,则由A口进气,在烧瓶中可收集到的气体
(2)若烧瓶中充满水,可收集到的气体是
这时气体由 口进入
(3)若烧瓶中装入浓硫酸进行气体干燥,则不能用该装置干燥的气体是
干燥其它气体时由 口进入
(4)若烧瓶是干燥的,不能用此装置来收集的气体是 ,其原因是
(用化学方程式表示)

查看答案和解析>>
科目: 来源: 题型:
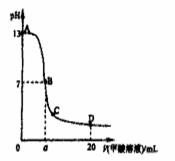
向15mL 0.1mol·L-1KOH溶液中逐滴加入0.2 mol·L-1甲酸(HCOOH,一元弱酸)溶液,溶液pH和加入的甲酸的体积关系曲线如右图所示,有关粒子浓度大小关系正确的是:
A.在A、B间任意一点c(K+) > c(HCOO-) > c(OH-) > c(H+)
B.在B点:c(K+) = c(HCOO-) > c(OH-) = c(H+),且a=7.5
C.在C点:c(HCOO-) > c(K+) > c(OH-) > c(H+)
D.在D点:c(HCOO-) + c(HCOOH) > 2c(K+)
查看答案和解析>>
科目: 来源: 题型:
有一种酸式盐AHB,它的水溶液呈弱碱性。则以下说法:①相同物质的量浓度的AOH溶液和H2B溶液,前者的电离程度大于后者的电离程度;②H2B不是强酸;③HB-的电离程度大于HB-的水解程度;④该盐溶液的电离方程式一般写成:AHB=A++HB-,HB-=H++B2-其中错误的是:
A.①② B.③④ C.②③ D.①④
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,正确的是:
A.pH=3和pH=4的盐酸各10mL混合,所得溶液的pH=3.5
B.溶液中c(H+)越大,pH值也越大,溶液的酸性就越强
C.液氯虽然不导电,但溶于水后导电情况良好,因此,液氯也是电解质
D.当温度不变时,在纯水中加入强碱不会影响水的离子积常数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com