
科目: 来源: 题型:阅读理解
工业生产的纯碱中常含有少量NaCl杂质。为测定某纯碱样品的纯度,化学课外活动小组设计了三种实验方案:
【方案一】取样品溶解后,加试剂使CO32-沉淀,测定沉淀的质量。
【方案二】用0.100 mol/L盐酸滴定。
【方案三】用稀酸将CO32-转化为CO2,测定CO2的质量。
解答31-34小题:
方案一的操作步骤有:①称量并溶解样品;②加入足量的BaCl2溶液;③过滤;④洗涤;⑤干燥;⑥称量并进行恒重操作。称量时所需定量实验仪器为____________________。判断是否达到恒重的标准是_____________________________________________________。
方案二的具体过程为:
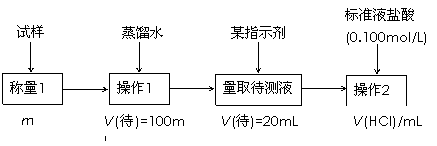 |
①操作1所需要的仪器有_____________________________________________。
②滴定时选择的指示剂为甲基橙。当溶液____________________________________时,说明达到了滴定终点。
③为减少偶然误差,通常的处理办法是_______________________________。
④滴定时若锥形瓶内有少量液体溅出,则测定结果_________。(选填“偏高”、“偏低”、“不影响”,下同),若盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗,测定结果_________。
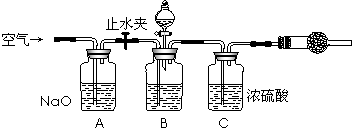 方案三的实验装置如下图:
方案三的实验装置如下图:
操作步骤有:①检查装置的气密性;②在干燥管内装满碱石灰,称量质量为W1 g;③称量W2 g样品装入广口瓶B中;④关闭止水夹;⑤缓慢加入稀H2SO4至不再产生气体为止;⑥ 打开止水夹;⑦缓缓鼓入空气数分钟,再称量干燥管,质量为W3 g。
该方案样品中纯碱的质量分数为__________________________(用代数式表示)。
上图中装置A的作用是_____________________。装置C的作用是_____________________。有同学认为空气中的水蒸气会进入干燥管导致测量结果_____________(填“偏大”、“偏小”或“无影响”)。改进措施可以是______________________________________________。
若用下图装置对样品进行分析,根据量瓶中收集到的液体的体积来计算样品中碳酸钠的含量。则下列装置中,最合理的是______。(选填序号)
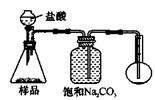
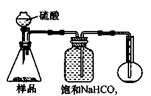
A B


C D
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C为同一短周期的三种元素,它们的原子序数依次增大且和为40;A是该周期中(除稀有气体元素外)原子半径最大的元素,B元素的原子核外M层上的电子数比K层上的电子数多1。解答26-30小题:
26.A原子的结构示意图为__________;A元素在周期表中位置为_____________________。
27.写出B的最高价氧化物与A的最高价氧化物对应水化物的溶液之间反应的离子方程式_______________________________________。
28.A和C形成的化合物的电子式为_____________,该化合物的水溶液呈__________性(填“酸”或“碱”)。
29.A是该周期中(除稀有气体元素外)原子半径最大的元素,从原子结构上看其原因是
________________________________________________。A、B、C三元素形成简单离子的半径大小顺序为____________。(用离子符号表示)
30.比较A、B单质活泼性的实验方法是__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
向MgC12和A1C13的混合溶液中加入氢氧化钠溶液,所得沉淀的物质的量(n)与加
入氢氧化钠溶液的体积(V)关系如右图所示。则下列说法正确的是( )
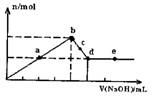
A.a、c两点沉淀物成份相同,d、e两点沉淀物成份相同
B.b点溶液的中c(Na+)=c(C1—)
C.b-c段与c-d段溶液中阴离子的物质的量相等
D.在d点,向溶液中加入少量盐酸,沉淀量将减少
查看答案和解析>>
科目: 来源: 题型:
下列事实能说明碳与硫两元素非金属性相对强弱的有( )
A.同条件同浓度溶液pH:Na2CO3>Na2SO4 B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价 D.分解温度:CH4>H2S
查看答案和解析>>
科目: 来源: 题型:
某次硫酸铜晶体结晶水含量的测定实验中,相对误差为-2.67%,其原因可能是( )
A.实验时盛放硫酸铜晶体的容器未完全干燥
B.加热过程中晶体有少量溅失
C.硫酸铜晶体中含有不分解失重的杂质
D.加热后固体未放入干燥器中冷却
查看答案和解析>>
科目: 来源: 题型:
某元素最高价氧化物化学式为RO2,其中R元素的质量分数为27.27%。对此元素叙述正确的是( )
A.该元素是第二周期ⅣA族的元素
B.该元素所形成的气态氢化物中含H量一定为25%
C.RO2与水反应能生成强酸
D.石油的成分主要是该元素与氢形成的化合物
查看答案和解析>>
科目: 来源: 题型:
等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加入相等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能是( )
A.甲、乙中都是铝过量 B.甲中铝过量、乙中碱过量
C.甲中酸过量、乙中铝过量 D.甲中酸过量、乙中碱过量
查看答案和解析>>
科目: 来源: 题型:
右图为周期表中短周期的一部分,若a原子最外层电子数比次外层电子数少3个,下说法中不正确的是( )
d | ||
a | b | c |
A.原子半径大小顺序是c>b>d>a
B.d的氢化物比a的氢化物稳定
C.a和d的原子结合可以形成带3个负电荷的阴离子
D.a、b、c最高价氧化物对应水化物的酸性强弱关系是c>b>a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com