
科目: 来源: 题型:
鉴别甲烷、一氧化碳和氢气三种无色气体的方法,是将它们分别( )
A.先后通入溴水和澄清的石灰水
B.点燃后罩上涂有澄清石灰水的烧杯
C.点燃、先后罩上干燥的冷烧杯和涂有澄清石灰水的烧杯
D.点燃后罩上涂有澄清石灰水的烧杯,通溴水
查看答案和解析>>
科目: 来源: 题型:
下列有机物不是同一种物质的是( )
A.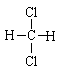 和
和 B.CH2=CH—CH=CH2和
B.CH2=CH—CH=CH2和 ![]()
C.C(CH3)3C(CH3)3和CH3(CH2)3C(CH3)3 D. 和
和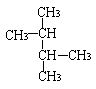
查看答案和解析>>
科目: 来源: 题型:
下列性质中属于烷烃特征性质的是( )
A.燃烧产物只有二氧化碳和水 B.分子通式为CnH2n+2,与氯气发生取代反应
C.它们是非电解质 D.它们几乎不溶于水
查看答案和解析>>
科目: 来源: 题型:
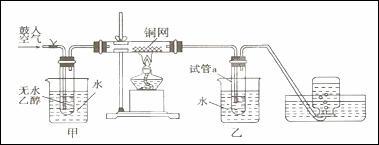
某实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式______________________、______________________。
⑵在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是 反应。
⑶若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 。要除去该物质,可在混合液中加入 (填写字母)。
A.氯化钠溶液 B.苯 C.碳酸氢钠溶液 D.四氯化碳
然后,再通过 (填实验操作名称)即可除去。
查看答案和解析>>
科目: 来源: 题型:
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加
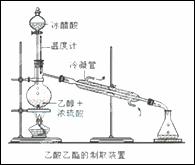 入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(
入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(
使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏(如下图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
(已知:乙醇、乙酸、乙酸乙酯的沸点依次是78.4℃、118℃、77.1℃)
(1)在烧瓶中加入一定比例的乙醇和浓硫酸的方法是:
。
(2)在该实验中,若用1mol乙醇和1mol 乙酸在浓硫酸作用下加热,充分反应,生成乙酸乙酯的物质的量小于1mol,原因是 。
(3)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
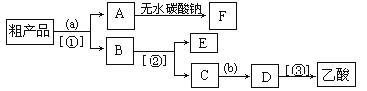
试剂a是__________;分离方法①是_________________,
分离方法②是__________________,分离方法③是_______________。
(4)在得到的A中加入无水碳酸钠粉末,振荡,是 。
查看答案和解析>>
科目: 来源: 题型:
燃烧法是测定有机化合物化学式的一种重要方法。在一定温度下取0.1 mol某液态烃A在O2中完全燃烧,生成CO2和水蒸汽,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重16.2 g,碱石灰增重35.2 g。
(1)写出烃A的分子式 ;
(2)含三个甲基的烃A同分异构体的数目为 ;
(3)烃A的一种同分异构体,其一氯代物只有一种,写出该同分异构体的结构简式 ;
查看答案和解析>>
科目: 来源: 题型:
现有A、B、C、D四种元素,A元素形成的—2价阴离子比氦原子的核外电子数多8个,B元素形成的一种化合物为淡黄色固体,该固体遇到空气能生成A的单质;C为原子核内有12个中子的金属元素,当2.4g C与足量热水反应时,在标准状况下放出气体2.24L,C形成正二价阳离子;D元素原子的M层上有7个电子。
(1)写出C的元素符号:C ;
(2)指出D在周期表的位置: ;
(3)B的最高价氧化物的水化物的电子式为 ,所含的化学键类型为 ;
(4)D的气态氢化物、H2S、HF的热稳定性由强到弱顺序是: (用化学式表示);
查看答案和解析>>
科目: 来源: 题型:
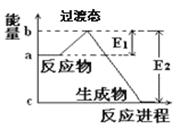
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能
量变化示意图,说明这个反应是 (填“吸热”或“放热”)反应,NO2和CO的总能量 (填“>”、“<”或“=”)CO2和NO的总能量。
(2)在某体积为2L的密闭容器中充入0.5mol NO2和1mol CO,在一定条件下发生反应:NO2+CO![]() CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
CO2+NO,2 min时,测得容器中NO的物质的量为0.2 mol ,则:
①该段时间内,用CO2表示的平均反应速率为 。
②假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量为 。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.容器内气体的质量保持变 B.NO2的物质的量浓度不再改变
C.容器内气体的平均相对分子质量不变 D.NO2的消耗速率与CO2的消耗速率相等
E.容器内气体的物质的量保持不变
查看答案和解析>>
科目: 来源: 题型:
![]() 哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充人1molN2和3molH2,在一定条件下使该反应发生,有关说法正确的是( )
哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充人1molN2和3molH2,在一定条件下使该反应发生,有关说法正确的是( )
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,单位时间里每增加1molN2,同时增加3molH2
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应的速率都为零
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com